武汉枢密脑科学技术有限公司品牌商
8 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.8999999999999999
- 1.9
- 0.8999999999999999
- 3.9
脑立体定位注射技术服务
询价
品牌商
武汉枢密脑科学技术有限公司
入驻年限:8 年
- 联系人:
枢先生
- 所在地区:
湖北 武汉市 江夏区
- 业务范围:
抗体、试剂、细胞库 / 细胞培养、技术服务、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 经销商
推荐产品
公司新闻/正文
Science Advances快讯 | 血脑屏障胶质细胞自闭症相关的基因突变造成睡眠障碍
1312 人阅读发布时间:2023-06-13 14:05

1.CHD8、CHD7和kismet基因突变的个体存在睡眠障碍
研究人员首先收集临床患者的睡眠数据,发现与自闭症患者相比,CHD8突变患者出现入睡困难且睡后醒来的频率明显增加,难以维持睡眠状态。接着研究人员选择了一个小队列,研究CHD8和CHD7突变患者的睡眠状态,发现突变患者均出现入睡困难和难以维持的状态。果蝇中kismet是CHD8和CHD7的同源基因,研究人员构建kismet突变的果蝇,发现果蝇也存在睡眠障碍。
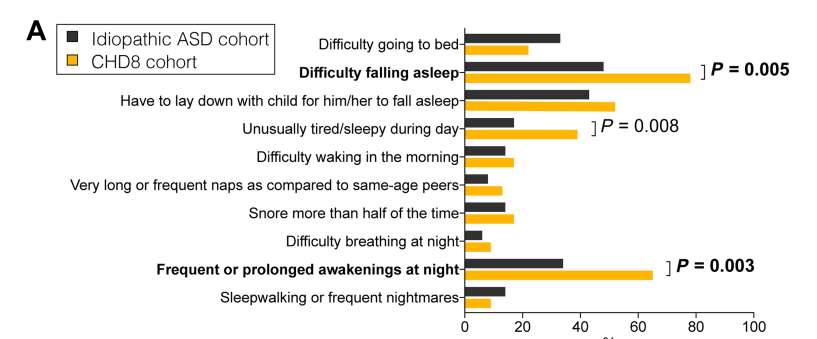
Figure 1. CHD8基因突变患者存在入睡困难和觉醒增加
2.敲除神经胶质细胞的kismet导致睡眠减少和碎片化
为了研究kismet在睡眠连续性中的作用,研究人员在中枢不同的细胞系上敲除kismet,发现神经元上敲除kismet并不影响果蝇的睡眠,但是在胶质细胞中敲除kismet导致夜间睡眠减少和睡眠碎片化增加。
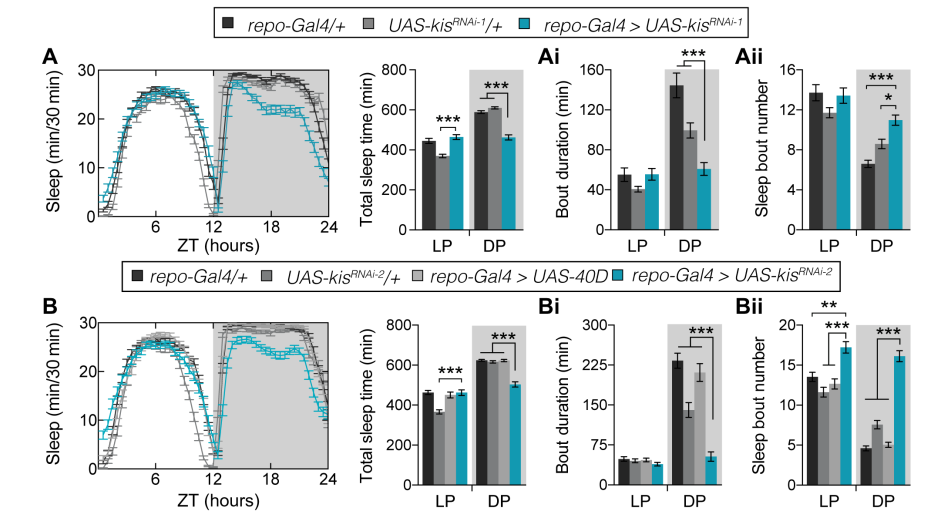
Figure 2.敲除神经胶质细胞的Kismet导致睡眠时间减少和睡眠碎片化
3、血脑屏障周围胶质细胞中的kismet保持睡眠的连续性
接着研究不同类型胶质细胞中kismet的作用,发现在星形样胶质细胞(ALG)中敲除kismet会出现睡眠碎片化,而在皮质胶质细胞和鞘内神经胶质细胞敲除不会出现睡眠碎片化。进一步研究发现神经外膜下胶质细胞(SPG,果蝇血脑屏障重要组成部分)中敲除kismet出现睡眠减少和碎片化增加。
接着研究不同类型胶质细胞中kismet的作用,发现在星形样胶质细胞(ALG)中敲除kismet会出现睡眠碎片化,而在皮质胶质细胞和鞘内神经胶质细胞敲除不会出现睡眠碎片化。进一步研究发现神经外膜下胶质细胞(SPG,果蝇血脑屏障重要组成部分)中敲除kismet出现睡眠减少和碎片化增加。
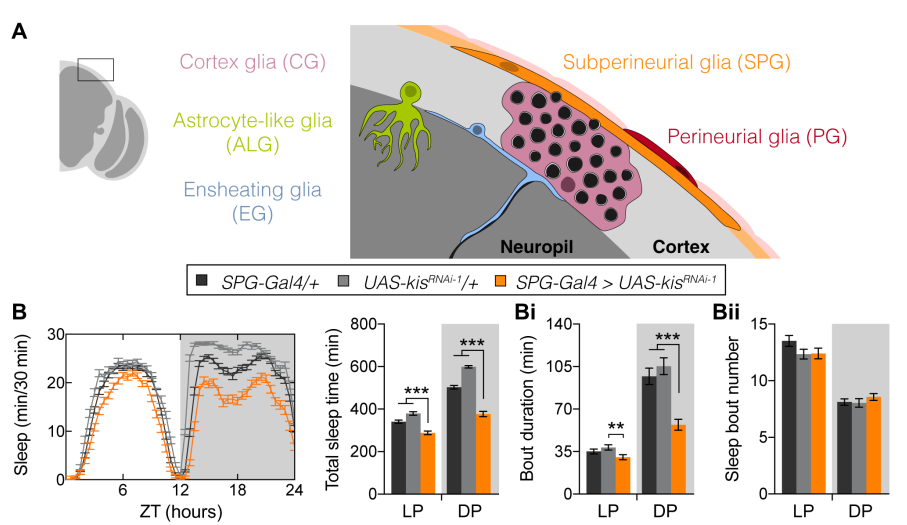
Figure 3.敲除神经周围胶质细胞的kismet减少睡眠时间和增加睡眠碎片化
4、敲除SPG中的kismet导致果蝇幼虫睡眠障碍
接着研究人员在果蝇幼虫的SPG中敲除kismet,对果蝇的睡眠进行检测。发现敲除kismet后不会改变睡眠的总时间,但是会破坏睡眠的结构,导致睡眠的时间减少,并且觉醒的次数增加。
5、胶质细胞敲除kismet导致5-羟色胺综合征
接着研究人员关注kismet功能不足导致睡眠障碍的原因,首先通过高效液相色谱研究5-HT的表达,发现敲除kismet夜晚5-HT表达大量增加。进一步研究发现敲除kismet会导致发育过程中5-HT表达的大量增加,进而导致睡眠障碍。
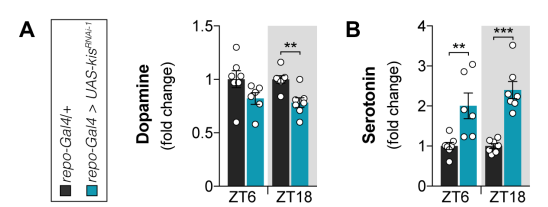
6、睡眠限制疗法改善胶质细胞kismet功能不足导致的睡眠障碍
接着研究人员希望找出改善胶质细胞kismet功能不足导致睡眠障碍的方案,以便能更好的运用于临床治疗。睡眠限制疗法是治疗慢性失眠的一线干预措施。研究人员将睡眠限制疗法运用于kismet功能障碍的果蝇模型,发现睡眠限制疗法能减少睡眠碎片化,维持良好的睡眠结构。
接着研究人员希望找出改善胶质细胞kismet功能不足导致睡眠障碍的方案,以便能更好的运用于临床治疗。睡眠限制疗法是治疗慢性失眠的一线干预措施。研究人员将睡眠限制疗法运用于kismet功能障碍的果蝇模型,发现睡眠限制疗法能减少睡眠碎片化,维持良好的睡眠结构。
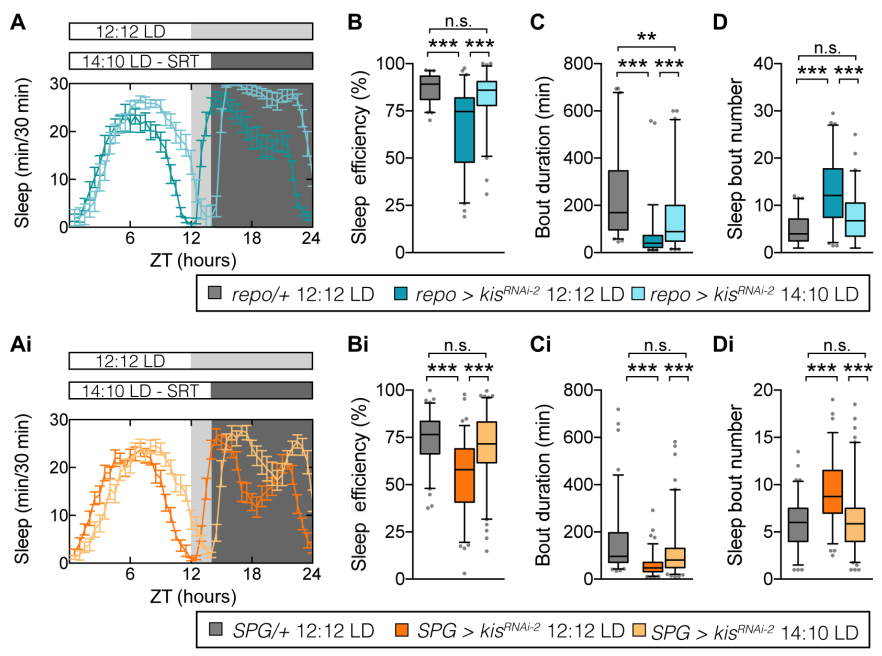
Figure 5.睡眠限制疗法改善胶质细胞kismet功能不足导致的睡眠障碍
7、CHD8和CHD7在人血脑屏障的胶质细胞高表达
最后为了确定kismet功能障碍导致的睡眠不足是否适用于临床。研究人员分析了人类皮质的单细胞RNA测序的数据集,发现CHD8和CHD7在人的血脑屏障细胞(放射样胶质细胞、星形胶质细胞、内皮细胞)中高表达。
徐老师点评
总而言之,本文研究人员通过临床案例,结合基因干预、免疫荧光,单细胞测序分析、果蝇的睡眠分析,发现血脑屏障胶质细胞中的CHD8/CHD7/Kismet基因突变,通过增加5-羟色胺介导睡眠障碍。本文将自闭症相关基因、血脑屏障胶质细胞、5-羟色胺综合征和睡眠障碍联系到了一起,并发现睡眠限制疗法有可能用于临床治疗神经发育障碍相关的睡眠问题。
图片来源:Science Advances
原文链接:http://advances.sciencemag.org/