武汉枢密脑科学技术有限公司品牌商
8 年
手机商铺
- NaN
- 0.09999999999999964
- 0.09999999999999964
- 1.0999999999999996
- 0.09999999999999964
武汉枢密脑科学技术有限公司
入驻年限:8 年
- 联系人:
枢先生
- 所在地区:
湖北 武汉市 江夏区
- 业务范围:
抗体、试剂、细胞库 / 细胞培养、技术服务、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 经销商
推荐产品
公司新闻/正文
IF=15.7【客户文章】耳朵一按就止痛?安医大张智/王海涛教授团队破解耳-脑轴镇痛神经环路,揭秘耳穴疗法现代神经生物学基础
57 人阅读发布时间:2026-05-06 09:35
《黄帝内经》记载“耳者,宗脉之所聚也”,传统中医依托耳部穴位刺激实现“脑病耳治”,为疼痛等神经系统疾病提供了无创干预思路。经皮耳迷走神经刺激(transcutaneous auricular vagus nerve stimulation,taVNS)作为耳穴刺激的现代转化技术,具备无创、安全、易操作等优势,在疼痛管理中展现出广阔临床前景。但当前taVNS发挥镇痛效应的核心现代生物学机制尚未阐明,严重限制了该技术的参数优化与临床规模化推广。
2026年4月,安徽医科大学/中国科学技术大学张智教授团队联合安徽医科大学口腔医学院王海涛教授、中国科学技术大学附属第一医院康芳教授及安徽医科大学口腔医学院王元银教授在Nature Communications发表题为“Auricular vagus nerve stimulation drives analgesia via an auricle–brain axis in a mouse model of neuropathic pain”的研究论文。该研究以神经病理性疼痛小鼠为模型,结合病毒示踪、深部钙成像、在体多通道电生理记录、光遗传学与化学遗传学等前沿技术,首次解析了taVNS通过耳-脑轴发挥镇痛作用的完整神经环路,为无创疼痛治疗提供了核心理论依据与精准干预靶点。

为明确taVNS的镇痛作用,研究人员构建保留性神经损伤(spared nerve injury,SNI)神经病理性疼痛小鼠模型,以左侧耳甲(迷走神经富集区)为靶点实施taVNS干预(3/15 Hz疏密波,持续30 min),同时以耳缘非迷走神经分布区刺激(tnVNS)作为阴性对照。行为学检测结果显示,taVNS干预后0.5 h即可诱导小鼠机械痛阈显著升高,产生急性镇痛效应,该效应在1.5 h后逐渐衰减;连续9天taVNS干预可产生稳定的慢性镇痛效果,停止刺激后镇痛作用仍可维持4天。此外,taVNS可有效缓解模型小鼠的冷痛异常敏化,在条件性位置偏好(CPP)实验中使小鼠对刺激配对环境产生显著偏好,同时减少冷刺激诱发的抬足等痛相关应对行为。与之对比,tnVNS干预在所有行为学检测中均未产生明显镇痛效应,证实taVNS的镇痛作用具有高度靶点特异性,仅激活耳甲迷走神经方可介导镇痛效应(图1)。
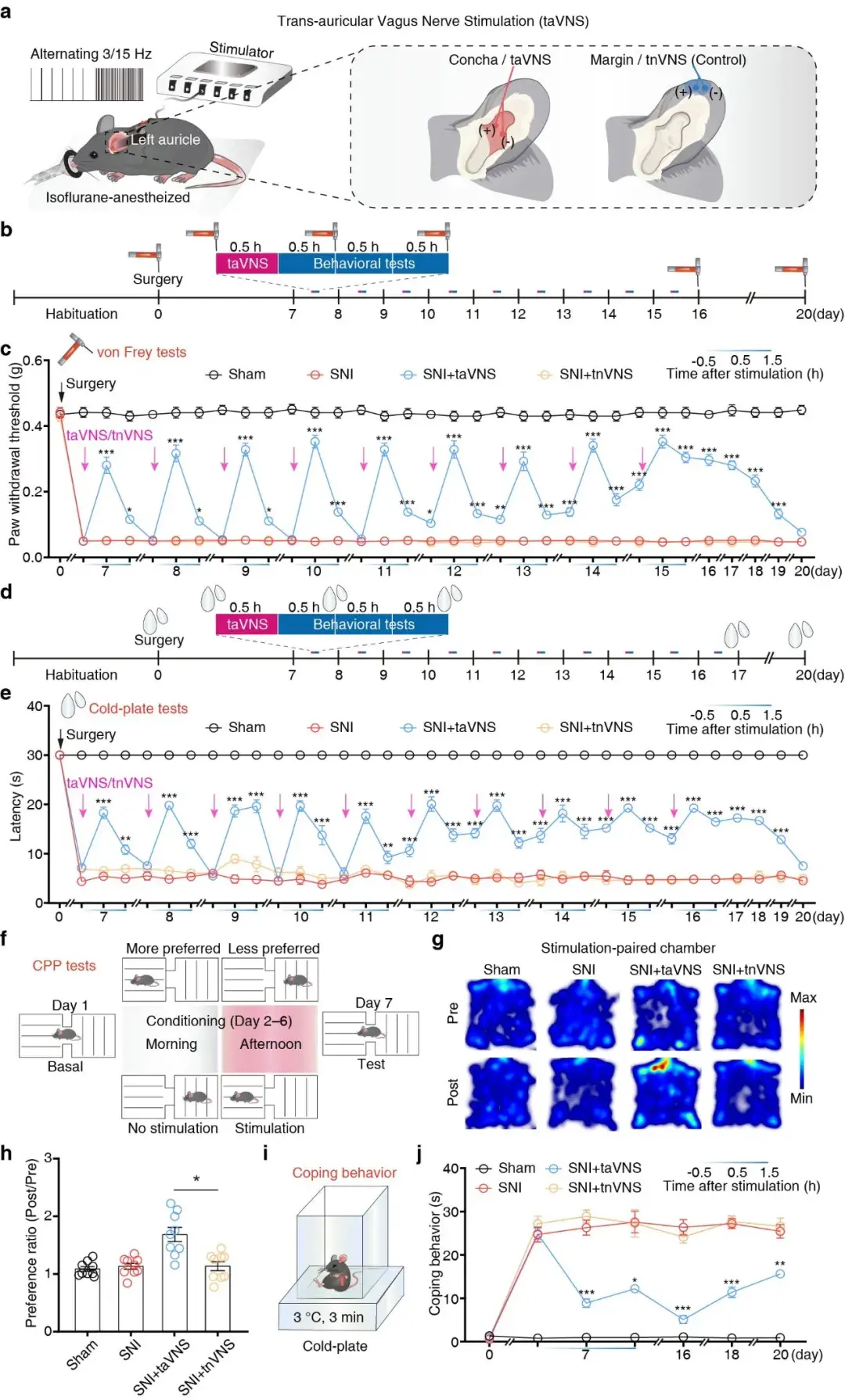
图1. taVNS在SNI模型小鼠上的镇痛效应。
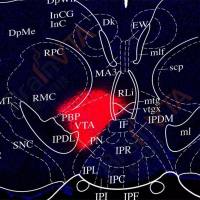
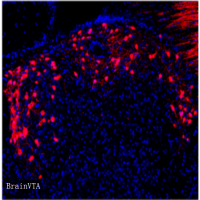
为揭示taVNS镇痛的神经解剖学基础,研究采用顺行与逆行病毒示踪技术,系统解析耳迷走神经传入的外周与中枢投射通路。顺行示踪结果表明,颈静脉-结状神经节(jugular-nodose ganglia,JNG)向耳甲区发出密集的迷走神经纤维,而在耳缘区域纤维分布极为稀疏;逆行示踪进一步证实,耳甲迷走神经支配JNG神经元,且该类神经元的中枢投射靶向孤束核(nucleus tractus solitarius,NTS)。荧光原位杂交结果显示,JNG内支配耳甲的感觉神经元存在分子异质性:颈静脉节神经元高表达Prdm12,结状节神经元高表达Phox2b,两类神经元均为谷氨酸能。双逆行示踪直接确认,JNG中存在同时支配耳甲与NTS的神经元群,明确了耳→JNG→NTS的直接解剖通路,为taVNS外周信号的中枢传入提供了确凿的解剖学证据(图2)。
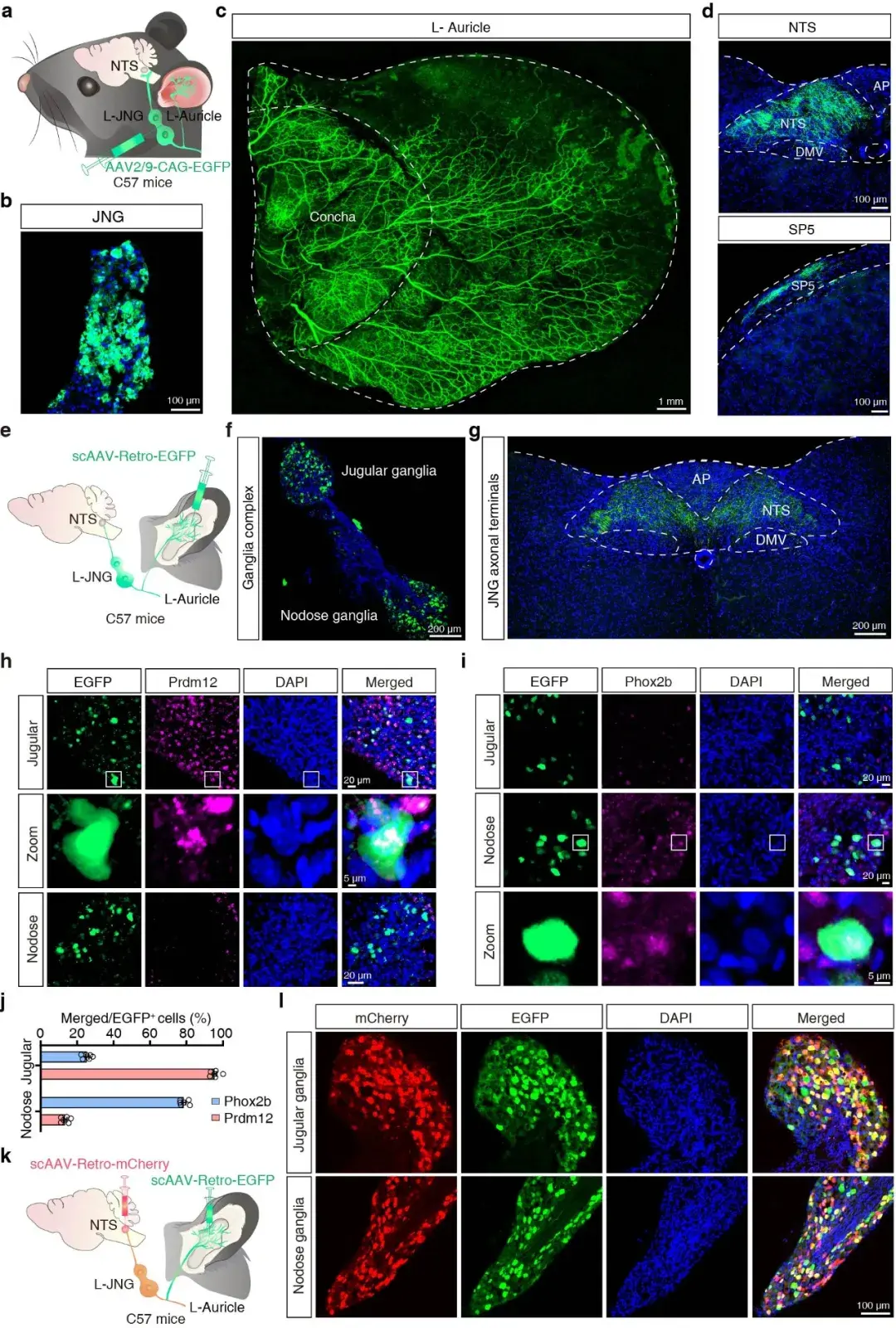
图2. 耳→JNG→NTS特异性投射通路解析。
为验证耳→JNG→NTS通路在taVNS镇痛中的功能必要性,研究结合光遗传、化学遗传与在体多通道电生理技术对该通路进行精准操控。在体多通道电生理记录显示,taVNS可显著增强NTS神经元自发放电频率。光遗传特异性激活耳→JNG→NTS通路的迷走神经中枢末梢,可完全模拟taVNS的急性与慢性镇痛效应,同时诱导CPP偏好、缓解冷痛异常相关行为;反之,化学遗传抑制该通路则完全阻断taVNS介导的镇痛作用。此外,光遗传直接激活耳甲处JNG外周纤维,可显著增强迷走神经与NTS的放电活动,并重现taVNS的全部镇痛表型。上述结果证实,耳→JNG→NTS通路是taVNS发挥镇痛作用的充分且必要通路(图3)。
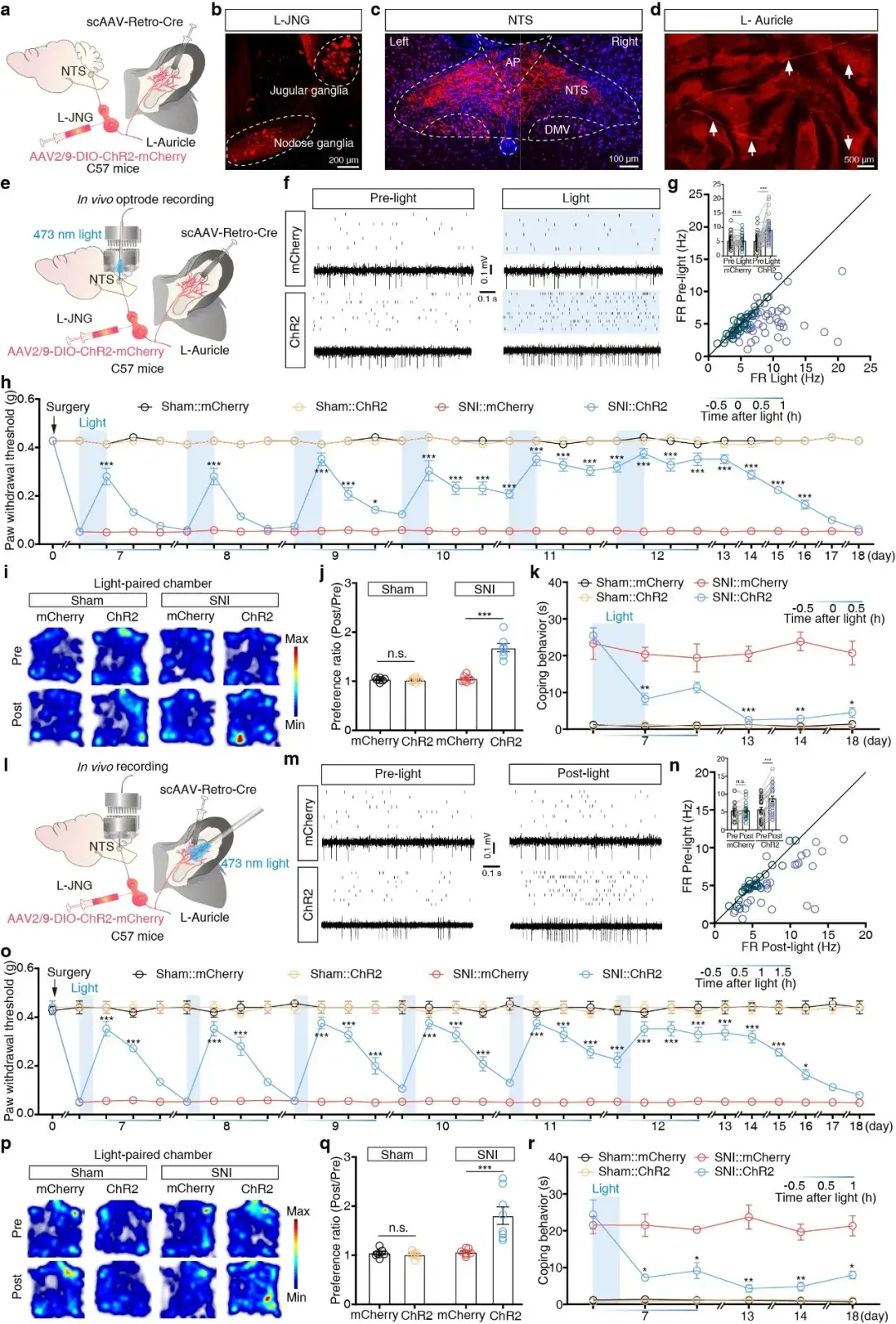
图3. 耳→JNG→NTS通路的激活是taVNS镇痛的充分和必要条件。
为定位NTS核团介导taVNS镇痛的关键细胞亚型,研究者通过病毒共定位、深部钙成像与行为学验证开展细胞特异性解析。病毒共定位结果显示,接收耳迷走传入的NTS神经元中,60.9%为阿黑皮素能(POMC)神经元,78.5%为谷氨酸能(Glu)神经元,GABA能神经元占比极低。深部钙成像结果显示,taVNS可特异性诱发NTSPOMC与NTSGlu神经元钙信号显著升高,对NTSGABA神经元激活作用微弱;光遗传激活耳迷走外周纤维可完全重现上述钙活动变化。行为学实验进一步证实,光遗传特异性激活接收耳迷走传入的NTSPOMC神经元,显著改善SNI小鼠的机械痛敏与冷痛异常,并诱导CPP效应。明确NTSPOMC神经元是taVNS在NTS核团发挥镇痛作用的核心细胞亚型(图4)。
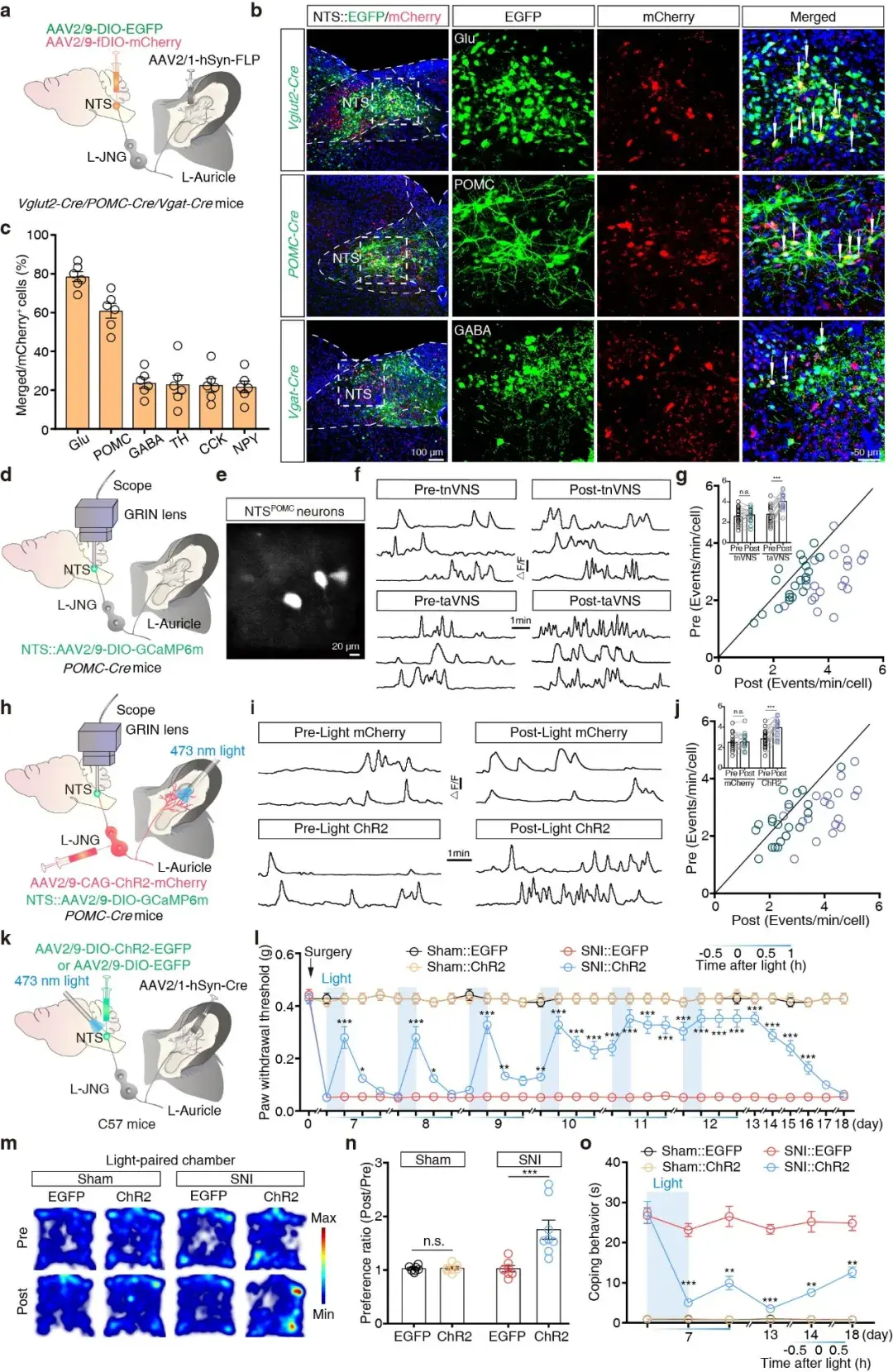
图4.NTSPOMC能神经元介导taVNS镇痛。
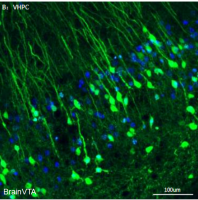
为探究NTSPOMC神经元的下游调控靶点,研究者通过顺行/逆行示踪、脑片膜片钳与化学遗传操控,系统解析其下游神经环路。顺行示踪结果显示,NTSPOMC神经元投射纤维主要富集于腹外侧导水管周围灰质(ventrolateral periaqueductal gray,vlPAG),同时少量投射至蓝斑(LC)、臂旁核(PBN)等镇痛相关脑区;免疫荧光共定位证实,vlPAG接收NTSPOMC投射的神经元主要为谷氨酸能神经元,且不表达磷脂酶Cβ4(PLCβ4)。脑片膜片钳结果显示,光遗传激活NTS投射至vlPAG的纤维末梢,在vlPAGGlu神经元上诱发出单突触兴奋性突触后电流(EPSC),证实二者形成直接兴奋性突触连接。功能实验表明,化学遗传特异性抑制投射至vlPAG的NTSPOMC神经元,可阻断taVNS诱导的机械镇痛与冷痛缓解效应,证明NTSPOMC→vlPAGGlu单突触通路是taVNS下行镇痛的关键环节(图5)。
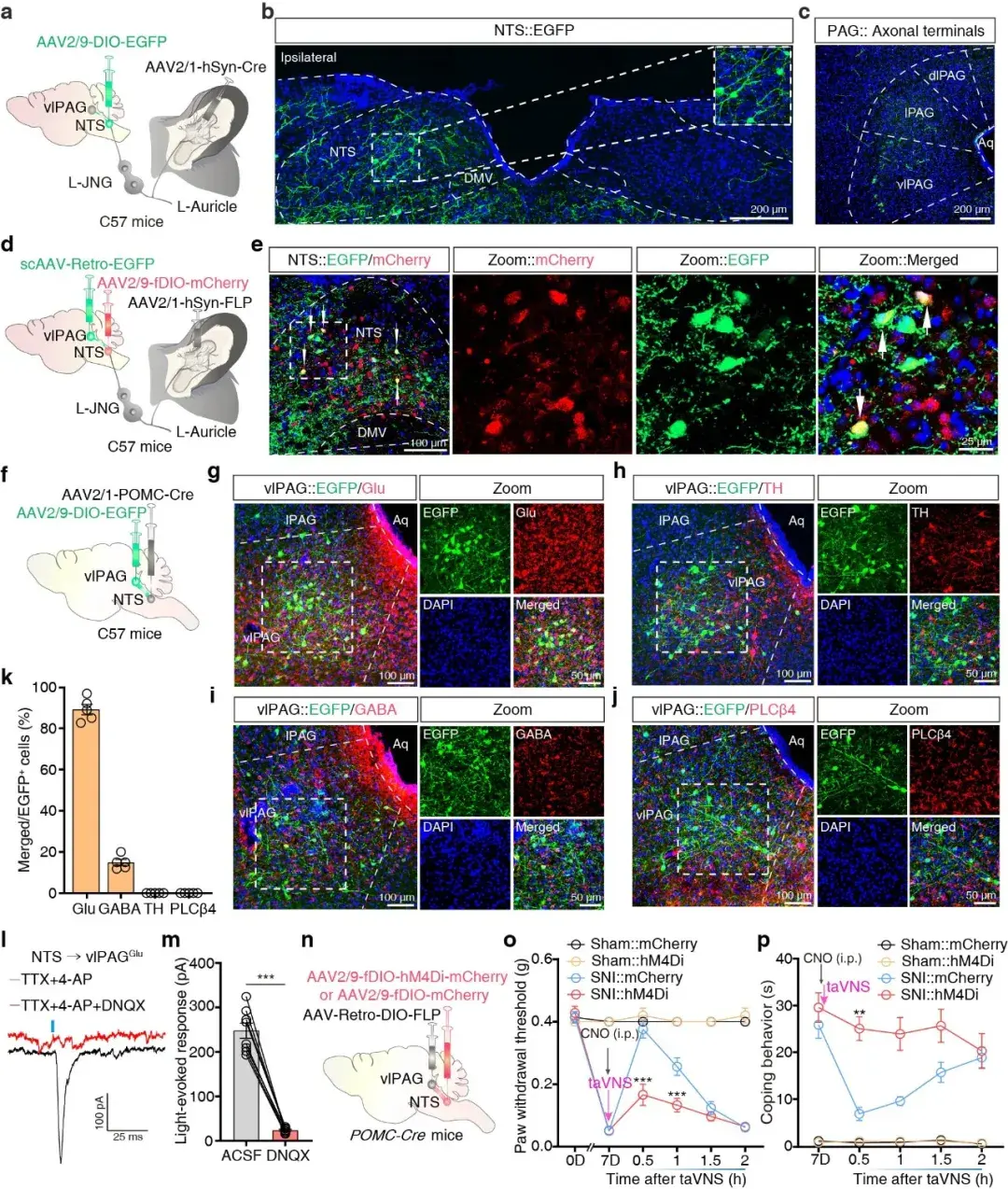
图5. NTSPOMC→vlPAGGlu通路是taVNS下行镇痛的关键环节。
为确认taVNS镇痛的完整级联通路,研究采用跨突触逆行示踪与双重组酶精准操控技术,对耳→JNG→NTS→vlPAG环路进行可视化验证与功能调控。跨突触逆行示踪直接可视化显示,耳甲迷走纤维、JNG神经元、NTS神经元与vlPAG神经元形成完整的四级神经环路连接,明确了该环路的解剖完整性。双重组酶策略特异性光激活接收耳迷走传入且投射至vlPAG的NTS神经元,可产生与taVNS完全一致的急性与慢性镇痛效应,并改善CPP与冷痛应对行为;化学遗传失活该类神经元则阻断taVNS的镇痛作用。同时,膈下迷走神经切断术证实,taVNS镇痛不依赖外周抗炎通路与儿茶酚胺释放,而是由上述“耳—脑”轴环路独立介导。最终证实,耳→JNG→NTS→vlPAG是taVNS发挥镇痛效应的完整功能性神经环路(图6)。
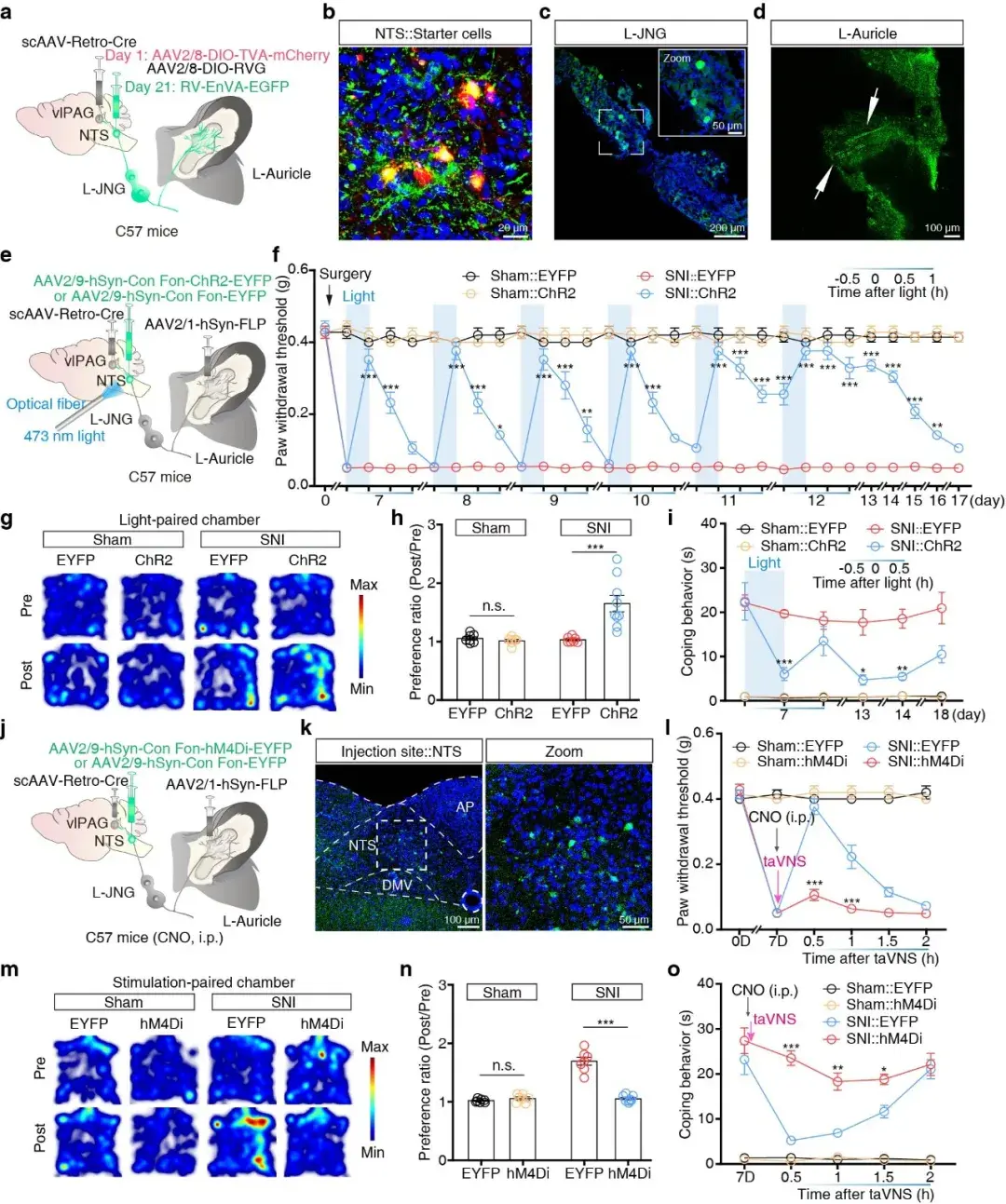
图6. 耳→JNG→NTS→vlPAG通路在taVNS镇痛中的作用。
结论
该研究发现,在神经病理性疼痛小鼠模型中,针对耳甲区实施taVNS可产生显著镇痛效应。具体机制为:耳郭迷走神经传入信号经JNG激活NTS的POMC神经元,进一步调控vlPAG的谷氨酸能神经元,最终启动内源性下行镇痛通路。该研究为taVNS在疼痛及其他神经系统疾病中的临床优化应用奠定了坚实理论基础,同时为中医药传统疗法的现代化、国际化进程贡献力量,促进了中西医结合领域的创新发展(图7)。
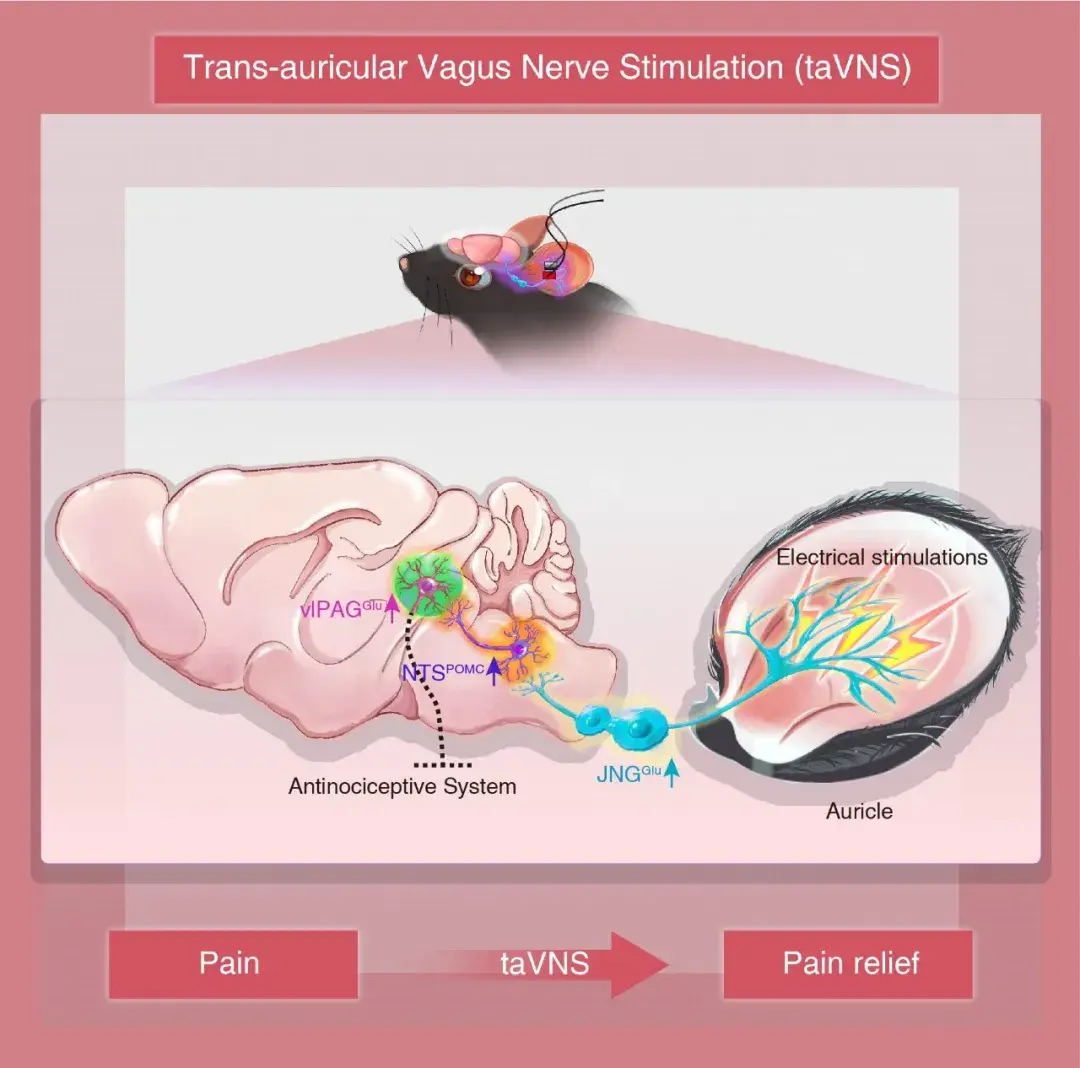
图7. taVNS通过“耳→JNGGlu→NTSPOMC→vlPAGGlu”的耳-脑轴神经环路,激活内源性下行镇痛系统。
安徽医科大学博士后彭晓琪、博士生刘业豪、中国科学技术大学博士生柳轶和毛云峰为论文的共同第一作者,安徽医科大学/中国科学技术大学张智教授为该论文的最后通讯作者,安徽医科大学口腔医学院王海涛教授、中国科学技术大学附属第一医院麻醉科康芳教授及安徽医科大学口腔医学院王元银教授为共同通讯作者。本研究得到安徽省中医药科技攻关专项项目、国家自然科学基金、科技创新2030—“脑科学与类脑研究”重大项目(中国脑计划)等项目的资助。

张智教授课题组合照
通讯作者介绍
张智,教授,博士生导师,安徽医科大学副校长,中国科学技术大学讲席教授。海外高层次引进人才,国家杰出青年基金获得者,科技创新2030——脑科学与类脑研究重大项目“中国脑计划”首席科学家,国家重点研发计划首席科学家;兼任中科院脑功能与脑疾病重点实验室主任、安徽省神经科学学会理事长等。张智教授课题组长期从事脑功能与脑疾病的病理学机制研究,系列性研究诠释了慢性疼痛的多维度新内涵,提出了疼痛多系统调控基础和临床转化研究的新模式,研究成果近5年以最后通讯作者发表于Science(2022/2026)、Nature Neuroscience(2019/2021/2024)、Neuron(2021)和Nature Metabolism(2022/2023)等期刊,入选中国神经科学重大进展(2021;2022)和Cell出版社中国年度最佳论文(2021)。
王海涛,安徽医科大学口腔医学院教授、博士研究生导师。长期从事感觉系统疾病的神经机制研究,先后主持国家自然科学基金等科研项目多项,研究成果近5年以通讯作者(含共同)发表在Science(2022)、Nature Communications(2026)、PNAS(2025)、Current Biology(2025)和Environmental Health Perspectives(2023)等国际学术期刊。
康芳,中国科学技术大学附属第一医院麻醉科主任医师,兼任中国心胸血管麻醉学会胸科麻醉分会委员、中国心胸血管麻醉学会日间手术麻醉分会委员、安徽省医师协会麻醉学分会委员。主要研究方向为疼痛敏感性及其与围术期镇痛、骨癌痛机制的基础研究。研究成果以第一/通讯作者(含共同)发表在Nature Communications(2026)和Nature Neuroscience(2021)等期刊。
王元银,教授、主任医师,博士研究生导师。现任安徽医科大学口腔医学院院长。安徽省“江淮名医”,安徽省特支计划创新领军人才和安徽省学术技术带头人后备人选。长期致力于口腔颌面外科相关疾病的诊断和治疗,专注口腔颌面部修复重建和三叉神经痛的发病机制及镇痛相关基础研究。主持国家自然科学基金及省部级科研项目10余项,以通讯/共同通讯作者在Nature Communications、Bioact.Mater.、Adv.Funct.Mater.和Adv.Sci.等期刊发表SCI论文50余篇,参编专著5部。

本文使用的来自枢密科技的病毒产品,列表如下:
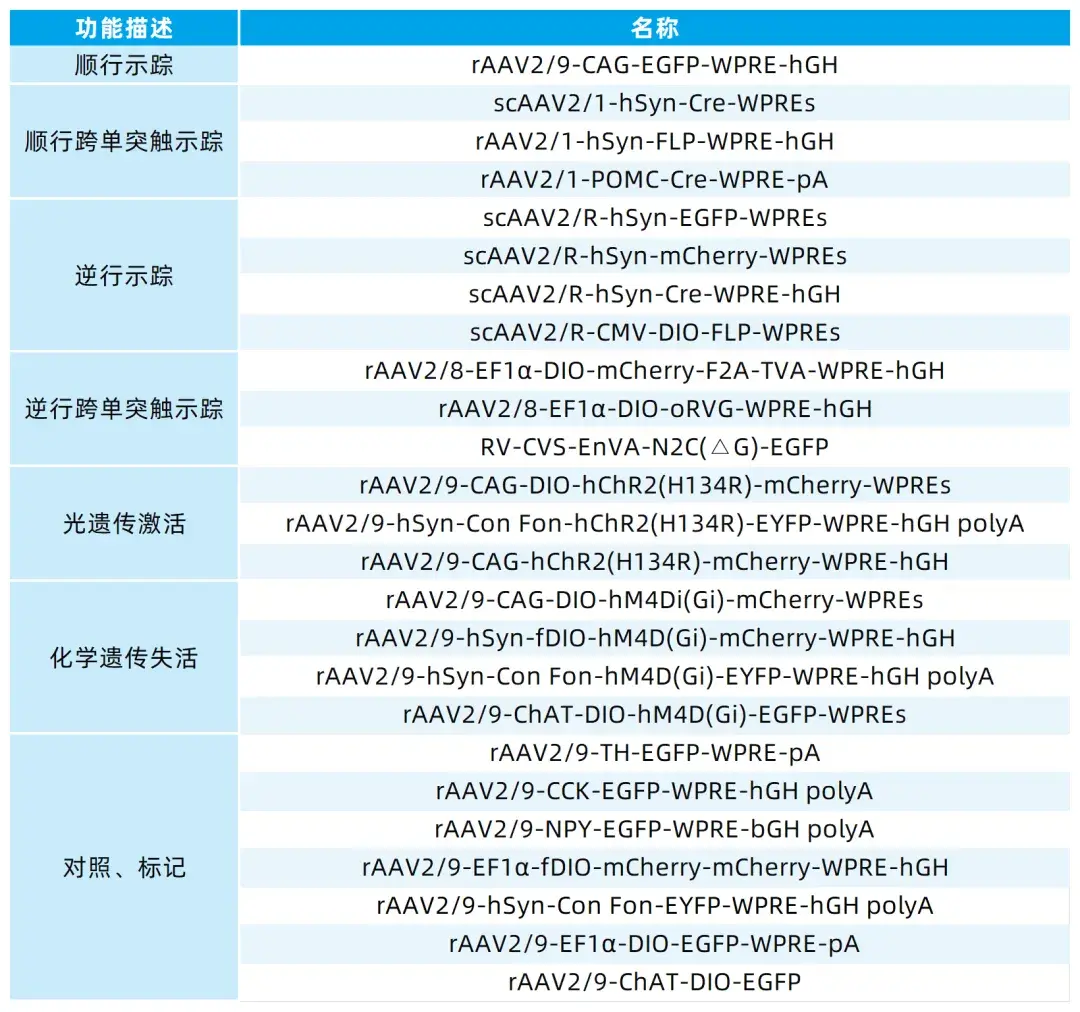
如有相关需求,或了解更多产品服务,欢迎咨询我们!点击进入店铺,查看更多产品及服务