武汉枢密脑科学技术有限公司品牌商
8 年
手机商铺
- NaN
- 0
- 0
- 1
- 0
武汉枢密脑科学技术有限公司
入驻年限:8 年
- 联系人:
枢先生
- 所在地区:
湖北 武汉市 江夏区
- 业务范围:
抗体、试剂、细胞库 / 细胞培养、技术服务、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 经销商
推荐产品
公司新闻/正文
【文献解读】Nature Neuronscience | 注意调控--vCA1 表达Htr2c 受体的神经元到EW CKK 神经元的投射
2273 人阅读发布时间:2023-08-04 11:18
基因科技的进步促进了神经元分类学的发展。科学家发现同一脑区形态上看似相同的神经元,因其基因表达的差异对行为的调节作用可能截然相反。研究某一类特定神经元与其他脑区之间的神经通路对行为的调节作用,已成为神经科学的大势所趋。
海马CA1分为背侧CA1(dCA1)和腹侧CA1(vCA1),这两个区域的神经投射和功能上存在较大的差异。啮齿类动物研究发现dCA1主要与大脑皮层形成相互联系,是学习和记忆的核心脑区。而vCA1锥体神经元分为wolfram syndrome 1(Wfs1)、transient receptor potential channel-4(Trpc4)和serotonin receptor 2c(Htr2c)三个亚群。其中,Trpc4神经元投射至伏隔核壳部、嗅球、基底内侧杏仁核,可储存社交记忆。Wfs1神经元与内嗅皮层形成突触连接,调节空间导航。而与Htr2c神经元相关的神经通路及其功能仍是未知的。
2018年8月14日,Nature集团旗下子刊《Nature Neuroscience》(2017年-2018年影响因子19.912)在线发表华中科技大学基础医学院/脑研究所鲁友明教授团队题为“Serotonin receptor 2c-expressing cells in the ventral CA1 control attention via innervation of the Edinger-Westphal nucleus”的研究论文,该论文回答了这一问题。论文中利用转基因小鼠结合病毒追踪技术、光遗传学技术、电生理记录和免疫荧光证实vCA1的Htr2c神经元与中脑的CKK-EW神经元形成功能性兴奋性神经通路。经行为筛选、病毒介导的蛋白表达干预、电生理记录、钙成像技术等方法发现该通路调节小鼠注意行为。此研究工作得到了国家自然科学基金创新研究群体、重大研究计划集成项目和重大仪器专项的资助。
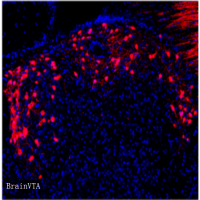
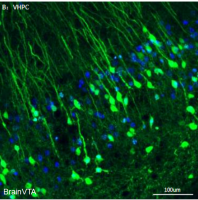
作者在Htr2c-Cre小鼠的双侧vCA1注射rAAV1/2-DIO-GFP病毒标记Htr2c阳性细胞,同时对Htr2c receptor(HR)进行免疫荧光染色,发现GFP与HR存在共定位(Fig. 1a-d),证实Htr2c-Cre转基因小鼠构建成功。随后作者发现vCA1的Htr2c神经元与兴奋性椎体神经元的标志物helix-loop-helix protein(NEX)存在共定位(Fig. 1e-f),而不与抑制性神经元的标志物glutamate decarboxylase 1 (GAD1)共定位。同时观察到vCA1的Htr2c神经元严格地分布在靠近起始层的海马锥体细胞层深层,区别于分布在靠近放射层的海马锥体细胞层表层的Wfs1神经元和Trpc4神经元。以上结果表明,vCA1的Htr2c神经元是兴奋性的。
为确保病毒干预Htr2c神经元的准确性,研究人员将Htr2c-Cre小鼠与mCherry-loxP小鼠进行杂交,得到全脑Htr2c神经元表达mCherry的Htr2cmCh小鼠(Fig. 1g)。在该小鼠双侧vCA1注射rAAV1/2-DIO-GFP病毒,发现GFP与mCherry共定位,表明该转基因小鼠能够用于研究Htr2c神经元并且病毒有较高的特异性。
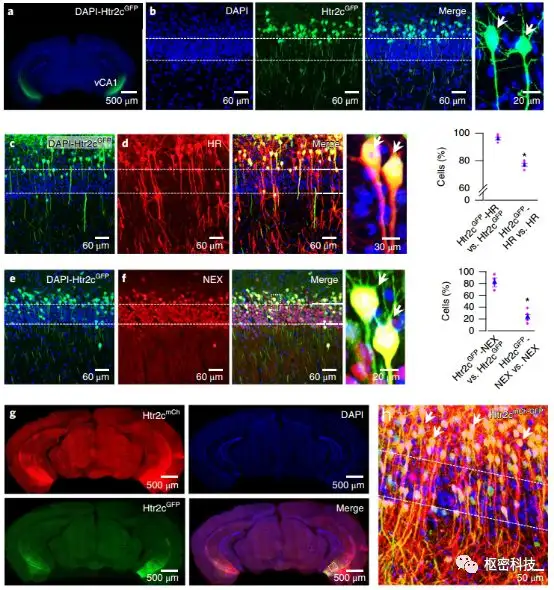
Fig1. vCA1的Htr2c神经元是兴奋性神经元
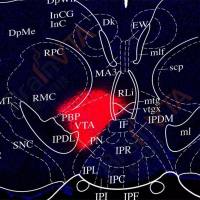
为了探究vCA1的Htr2c神经元下游投射,作者首先在Htr2c-Cre小鼠双侧vCA1注射rAAV1/2-DIO-TK-GFP,4周后在同一位点注射H129ΔTK-mCh(Fig. 2a-d),从而实现vCA1的Htr2c神经元顺行跨一级示踪。定量分析显示Edinger-Westphal nucleus(EW)的mCherry阳性细胞(即受vCA1的Htr2c神经元支配细胞)占全脑中所有mCherry阳性细胞的56%(Fig. 2e-g)。免疫荧光结果显示EW的mCherry阳性细胞为cholecystokinin(CCK)阳性(Fig. 2d)。
为了进一步确定vCA1Htr2c+ - EWCCK+之间的直接突触联系,作者在CCK-Cre小鼠EW注射rAAV1/2-DIO-TVA/G-GFP,4周后在同一位点注射ΔG-RV- mCh,从而实现EW的CCK神经元逆行跨一级示踪。免疫荧光结果显示vCA1的mCherry阳性细胞95%为Htr2c阳性,因此Htr2c神经元能够直接支配EW的CCK神经元。
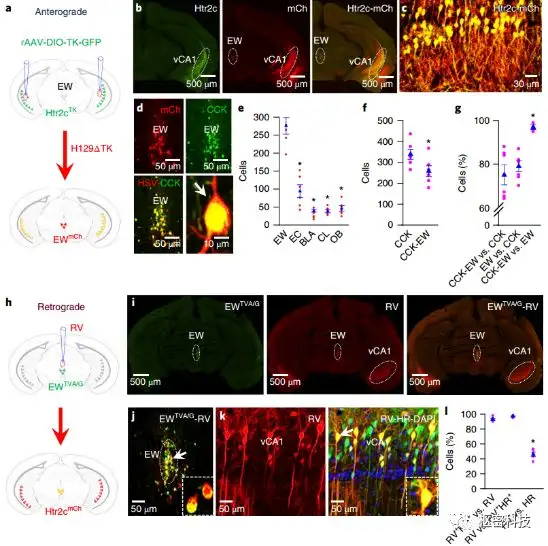
Fig2. vCA1的Htr2c神经元是兴奋性神经元
为了确定vCA1Htr2c+和EWCCK+之间的突触连接是否具有功能性,作者在Htr2c-Cre小鼠双侧vCA1注射rAAV1/2-DIO-ChR2-mCh,使得vCA1的Htr2c神经元表达光敏感蛋白ChR2(Fig. 3a-c)并且能够响应蓝光兴奋产生连续放电(Fig. 3d, e)。为了使EW神经元可视化,作者在Htr2cChR2小鼠的EW注射rAAV1 / 2-GFP使 EW细胞可视化(Fig. 3f),通过光照Htr2cChR2小鼠EW的vCA1传入轴突纤维诱发EPSCs。诱发的EPSCs随光照强度的增强而增加,在加入NMDA受体的拮抗剂AP5后EPSCs完全消失(Fig. 3g-h)。进一步分析发现EPSCs符合单一发放(Fig. 3i),且与单突触传递的电生理特性一致(Fig. 3j)。因此vCA1Htr2c+通过兴奋性单突触连接通路支配EWCCK+。
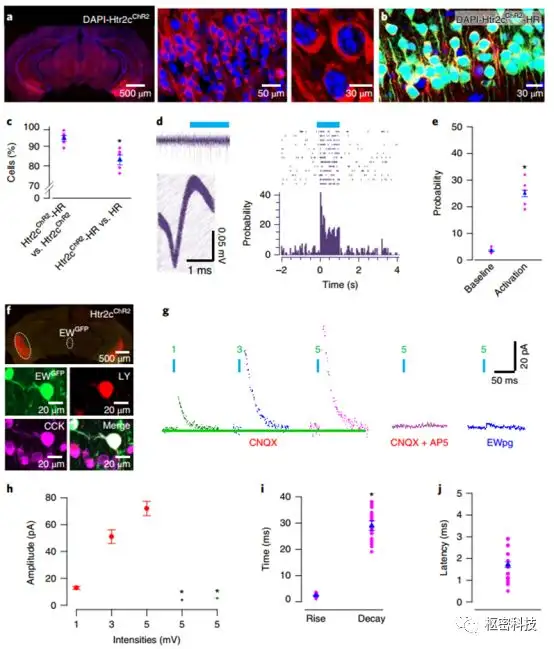
Fig3. vCA1Htr2c+和EWCCK+两者间是功能性单突触连接
为了研究Htr2c神经元活性依赖的神经功能,作者通过构建Htr2cKir2.1小鼠抑制Htr2c神经元功能。由于vCA1神经元调控注意行为,作者推断抑制Htr2c神经元可能会影响依赖注意力的行为表现。和Htr2cGFP小鼠相比,两组在运动能力、学习、记忆和情绪等行为中表现均无显著差异,而Htr2cKir2.1小鼠在5-CSRT (five-choice serial reaction-time)中正确率显著低于对照组小鼠(Fig. 4b)。视觉线索呈现0.5-2s(stimulus duration,SD),5-CSRT结果显示SD(stimulus duration)为1.5s时两组动物正确率、错误率及丢失率均无显著差异,而当SD为1s、0.5s时Htr2cKir2.1小鼠错误率及丢失率显著高于Htr2cGFP小鼠,因此抑制Htr2c 神经元减弱小鼠注意行为(Fig. 4c-e)
那么,借由光遗传激活Htr2cKir2.1小鼠Htr2c神经元是否可恢复注意力的损伤呢?将Htr2c-Cre小鼠分为4组分别于vCA1区域注射rAAV1/2-DIO-GFP-IRES-mCh病毒(Htr2cGFP-mCh)、rAAV1/2-DIO-GFP-IRES-ChR2-mCh病毒(Htr2cGFP-ChR2)、rAAV1/2-DIO-Kir2.1-IRES-mCh病毒(Htr2cKir2.1-mCh)和rAAV1/2-DIO-Kir2.1-IRES-ChR2-mCh病毒(Htr2cKir2.1-ChR2)。分别在双侧vCA1埋置光纤,在5-CSRT中予以5mW 473nm的蓝光激活(30–40Hz, 2-ms pulse) (Fig. 4g),激活Htr2c cells可提高动物在5-CSRT中的表现并恢复Kir2.1导致的注意力损伤(Fig. 4h-j)。
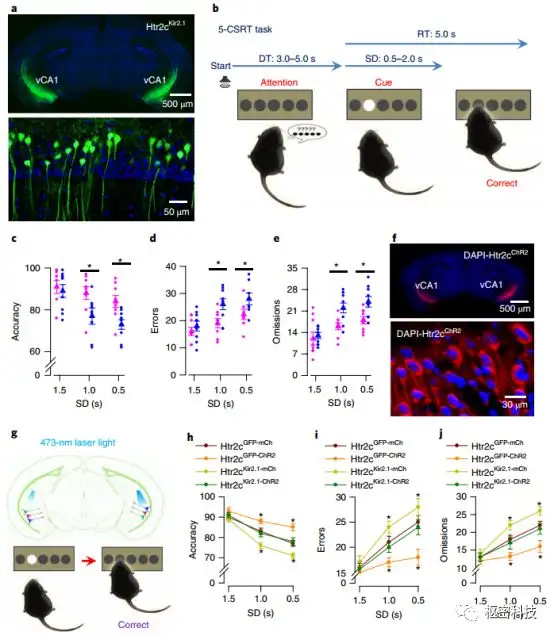
Fig4. 抑制Htr2c神经元减弱注意行为。
此外,本研究还通过钙信记录和单一神经元活动记录在5-CSRT中Htr2c神经元。CaMPARIloxP/loxP小鼠神经元内loxP/loxP位点经Cre重组酶剪切可启动CaMPARI表达(Fig. 5a)。CaMPARI表达后在激发光的照射下,一旦神经元内Ca2+增加,神经元便会由绿色荧光状态转换为红色荧光状态。因此,可记录CaMPARIloxP/loxP与Htr2c-Cre小鼠杂交的后代在5-CSRT中的动作电位发放率,在双侧vCA1埋置光纤予以7mW 405nm激光照射(Fig. 5b)可对任务中Ca2+增加的Htr2c神经元进行计数、统计。细胞计数结果显示,动物做出正确反应时Htr2c神经元激活,错误及丢失时Htr2c神经元Ca2+改变(Fig. 5c-f)。单一神经元活动记录结果与之前一致,当正确反应时Htr2c神经元发放率显著大于错误及丢失时(Fig. 5g-i)。上述实验可知,vCA1的Htr2c神经元参与调节注意行为。
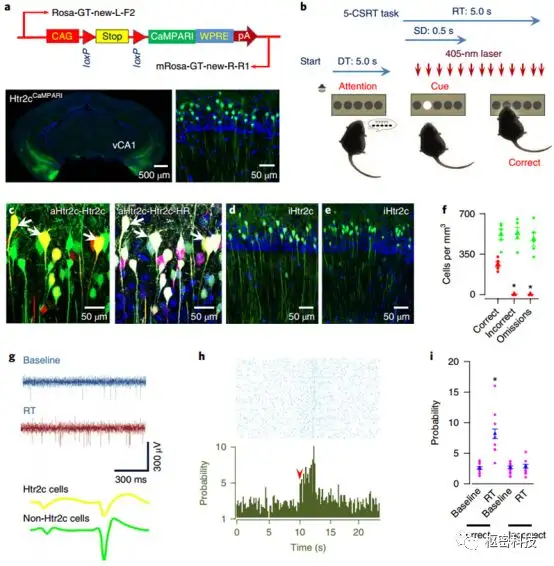
Fig5. 激活Htr2c神经元加强注意行为。
前文已经证明vCA1的Htr2c 神经元下行投射到EW,并且为功能性单突触连接。那么,vCA1Htr2c+ - EWCCK+通路是否参与注意调节呢?研究进一步揭示了该通路在注意调控中的作用。与之前的方法相同,iCCK-Cre小鼠EW区域注射rAAV1/2-DIO-Kir2.1-GFP,抑制EW区域CKK+神经元功能(Fig. 6a, b),发现EWKir2.1小鼠注意力下降(Fig. 6d-f)。
iCCK/Htr2c-Cre小鼠,分别在其vCA1注射rAAV1/2-DIO-ChR2, EW注射rAAV1/2-DIO-Kir2.1(Fig. 6g)。光纤埋置于EW附近,行为测试中给与蓝光(Fig. 6a, b),行为数据表明,EW功能受到抑制可阻断Htr2c神经元激活提高动物注意力。似乎EW 作为Htr2c的功能性输出,其活动决定了动物5-CSRT的行为表现。
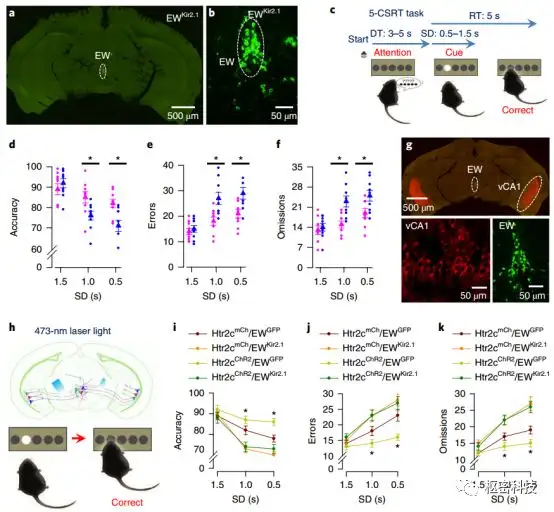
Fig6. 抑制EW神经元减弱注意行为。
假设如此,那么激活EW神经元,是否可恢复Htr2cKir2.1小鼠注意损伤呢?通过在iCCK-Cre/Htr2cKir2.1/GFP小鼠EW处注射rAAV1/2-DIO-ChR2-mCh(Fig. 7a),得到Htr2cGFP/EWmCh、Htr2cGFP/EWChR2、Htr2cKir2.1/EWmCh和Htr2cKir2.1/EWChR2四组实验小鼠。在行为测试中予以蓝光照射EW神经元(Fig. 7b),行为数据证实EW神经元对注意行为的决定性作用,激活EW神经元阻断了Htr2c处Kir2.1导致的注意力损伤(Fig. 6c-h)。对EW下游脑区进行逆向示踪及连接功能性功能性验证并通过光遗传操控,发现EW通过mPFC区域PV神经元调控注意行为,黄光抑制EW-mPFC通路动物注意任务中表现损伤(Supplementary)。
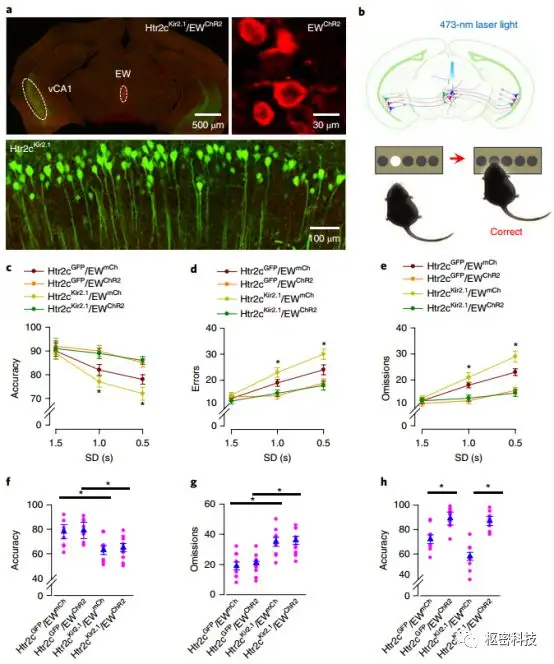
Fig7. 激活EW神经元加强注意行为。
如有相关实验需求,或了解更多产品服务,欢迎咨询我们!