武汉枢密脑科学技术有限公司品牌商
8 年
手机商铺
- NaN
- 0
- 0
- 1
- 0
武汉枢密脑科学技术有限公司
入驻年限:8 年
- 联系人:
枢先生
- 所在地区:
湖北 武汉市 江夏区
- 业务范围:
抗体、试剂、细胞库 / 细胞培养、技术服务、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 经销商
推荐产品
公司新闻/正文
【客户文章】Cell Reports | Men1基因缺失导致小鼠突触功能障碍和认知障碍。
689 人阅读发布时间:2023-08-04 11:19
CDK5是细胞周期蛋白激酶家族中的一个特殊成员。与其它细胞周期蛋白激酶均依赖于Cyclin所不同,CDK5是被在神经系统高表达的p35/p25蛋白所激活;因此CDK5在神经系统具有高特异的活性,并且与神经发育以及多种脑疾病的发生有着密切的关系。CDK5的缺失或功能低下会导致神经发育障碍;而CDK5的过度激活却会导致神经元死亡,被认为是导致阿尔茨海默病的一个关键因素。但是至今为止人们对神经系统中CDK5的上游调控机制了解甚少。张杰教授及其团队发现,在神经元中多发性内分泌肿瘤蛋白(menin)会通过调控表观遗传因子H3K4me3来调节CDK5激活蛋白p35基因的转录,从而调节CDK5的激酶活性。该研究成果不仅为更深入理解CDK5的调控和阿尔茨海默病(AD)的发病机制提供了新的思路,也为menin的研究打开了新的大门。
2018年7月17日,国际著名杂志《Cell》子刊《Cell Reports》在线发表了厦门大学医学院神经科学研究所张杰教授团队的最.新研究成果“Neuron-specific menin deletion leads to synaptic dysfunction and cognitive impairment by modulating p35 expression.”的研究论文。论文中利用Cre-LoXP技术得到全神经系统敲除及神经元特异性敲除Men1的模型,结合行为学实验、电生理记录、Microarray及免疫荧光等实验手段,证实神经元特异性敲除Men1的小鼠存在明显的记忆缺失,而这一现象与P35的表达缺失引起的CDK5激酶活性的抑制有关。该研究成果是与厦门大学神经科学研究所的许华曦教授、卜国军教授、张云武教授合作,并且在厦门大学医学院金光辉教授的大力支持下完成的。研究工作得到国家自然科学基金项目(81522016、81271421、31571055)以及厦门大学校长基金等资助。

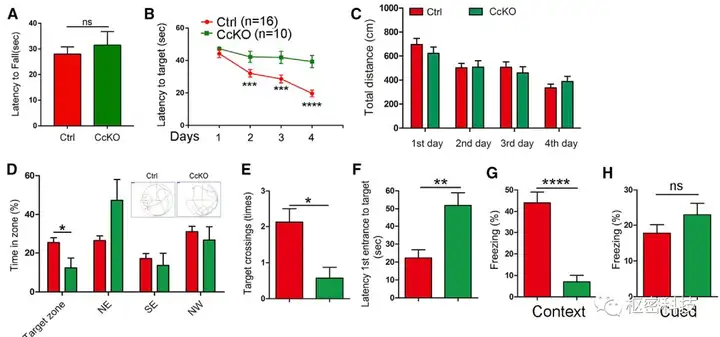
作者首先证实了Menin在神经系统中较高水平的表达,而后交配转基因小鼠获得Nestin;Men1F/F(NcKO)及CaMK2α-Cre;Men1F/F(CcKO)小鼠,因NcKO小鼠呈现出体型偏小,出生后致死的表型。故对CcKO小鼠进行认知相关行为学项目的分析,发现CcKO在水迷宫及条件惊恐Context测试中存在明显的差异,初步推测可能因神经元特异性缺失Menin造成海马依赖型的记忆受损。
作者紧接着在电生理水平上检测了CcKO小鼠的海马CA1-CA3的LTP、Input-output及PPR,发现CcKO小鼠的神经元功能受损主要是由于突触后兴奋性发放缺失造成。而后在生化水平上检测发现在CcKO小鼠的海马及原代神经元包括PSD95、GluR1和Synaptophysin等突触间标记物明显下降。结合Goigi staining分析,发现CcKO小鼠中神经元分支和突触数量减少。综上,受损的LTP很可能是由于功能型突触的减少和突触后功能缺失造成的。
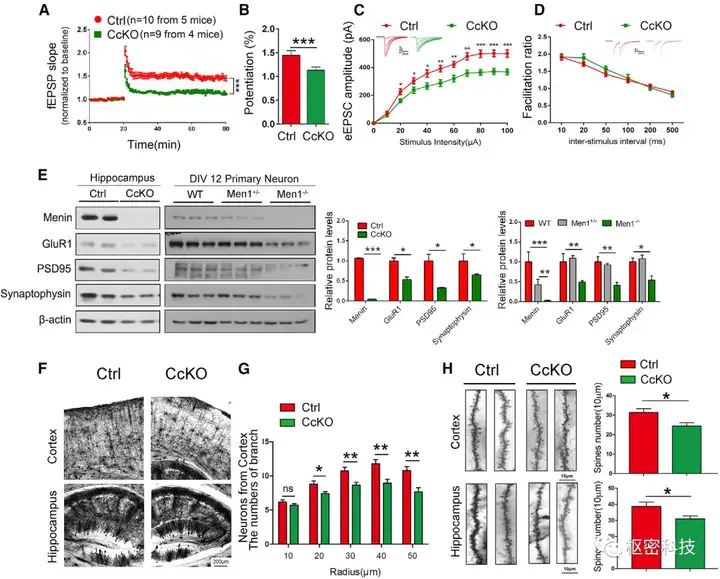
为了探寻Menin缺失造成的下游调控机制的紊乱,作者在N2a细胞系上瞬转Men1 siRNA后运用Microarray检测RNA水平的变化,发现Menin缺失造成了CDK5r1(p35)表达的缺失,并在N2a细胞系、NcKO及CcKO小鼠等样品验证。同时运用体外激酶实验发现CDK5在蛋白水平不变的情况下,蛋白激酶活性明显缺失。最后,运用ChiP及Luciferase assay证实,Menin会通过调控表观遗传因子H3K4me3来调节CDK5激活蛋白p35基因的转录,从而调节CDK5的激酶活性。
为了证实外源性p35是否能够缓解CcKO的认知及突触功能缺失,作者运用AAV病毒工具,对P0的CcKO小鼠两侧侧脑室注射AAV-CaMK2α-p35。两个月后,分别检测水迷宫、条件惊恐(Context)等行为学,发现外源性过表达p35能够缓解CcKO的认知缺陷。并在后续电生理及生理生化水平检测发现,p35能够通过改善突触功能缺失,使CcKO小鼠的认知损伤得以缓解。
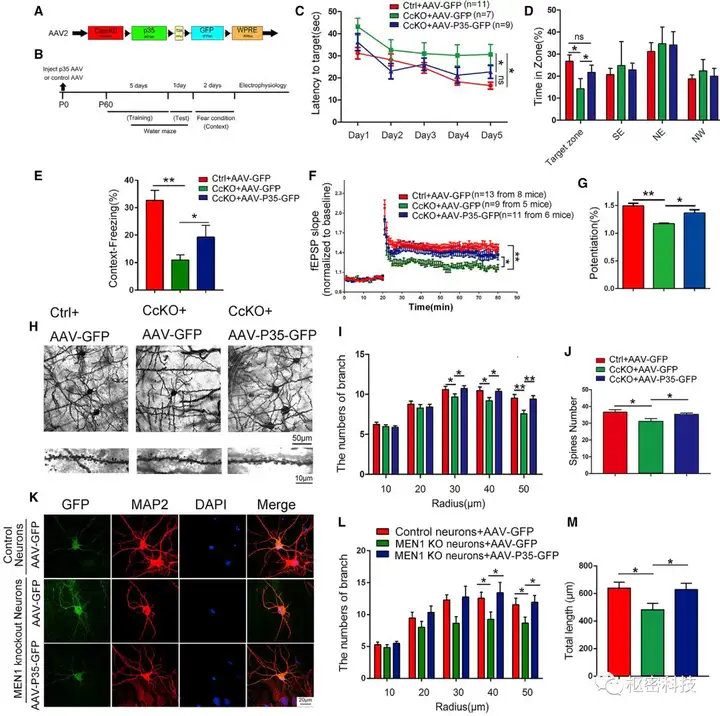
值得一提的是,与本文几乎“背靠背”发表的于《Neuron》上的“Menin deficiency leads to depressive-like behaviors in mice by modulating astrocyte-mediated neuroinflammation”结合证实了MEN1是抑郁症在中国人群中新的致病基因,并阐明了MEN1调控星形胶质细胞炎症导致抑郁发生发展的新机制,为抑郁症的诊治提供了新靶点和方向。

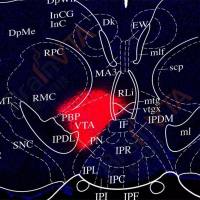
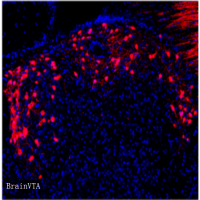
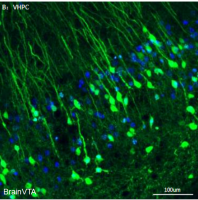
本文中运用了AAV-CaMK2α-p35-GFP及其对照病毒由枢密科技提供相应技术支持,前期验证中可以看到较好的表达,如下图:

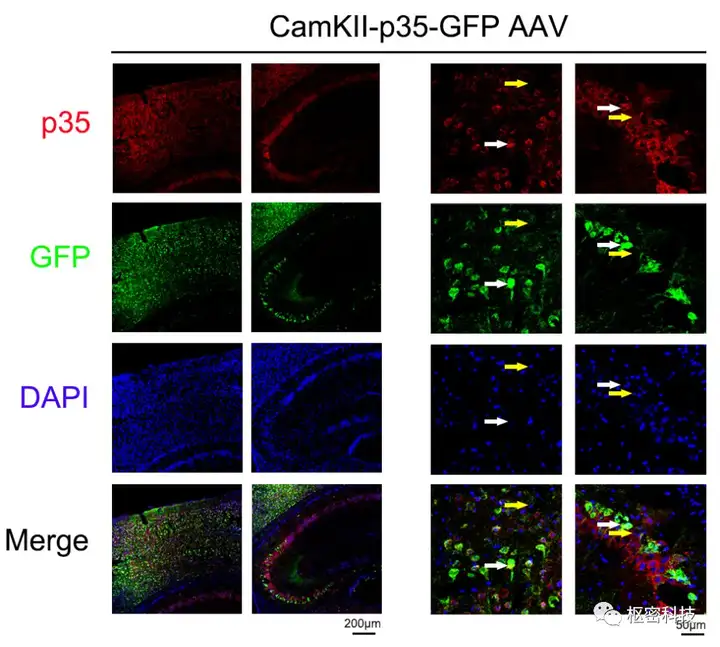
张杰,厦门大学特聘教授、博士生导师。国家优秀青年科学基金;教育部新世纪优秀人才;福建省杰出青年科学基金;厦门市五四青年奖章等获得者。2011年8月加入厦门大学医学院神经科学研究所担任教授至今。张杰博士主要从事重大神经系统疾病(老年痴呆、帕金森、抑郁症、自闭症、术后认知障碍、胶质瘤)等的发病机制和药物开发研究。至今以第一作者或者通讯作者在国际知名期刊发表研究论文21篇。其中回国独立开展研究工作以后,作为通讯作者在 Neuron,Cell Reports, PNAS, The Journal of Neuroscience, Clinical Cancer Research,Cell Death and Disease, JBC, Chemistry,Chem. Biol. Drug Des.等杂志上发表多篇研究论文。
如有相关实验需求,或了解更多产品和服务,欢迎咨询我们!