武汉枢密脑科学技术有限公司品牌商
8 年
手机商铺
- NaN
- 0.8999999999999999
- 1.9
- 0.8999999999999999
- 3.9
武汉枢密脑科学技术有限公司
入驻年限:8 年
- 联系人:
枢先生
- 所在地区:
湖北 武汉市 江夏区
- 业务范围:
抗体、试剂、细胞库 / 细胞培养、技术服务、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 经销商
推荐产品
公司新闻/正文
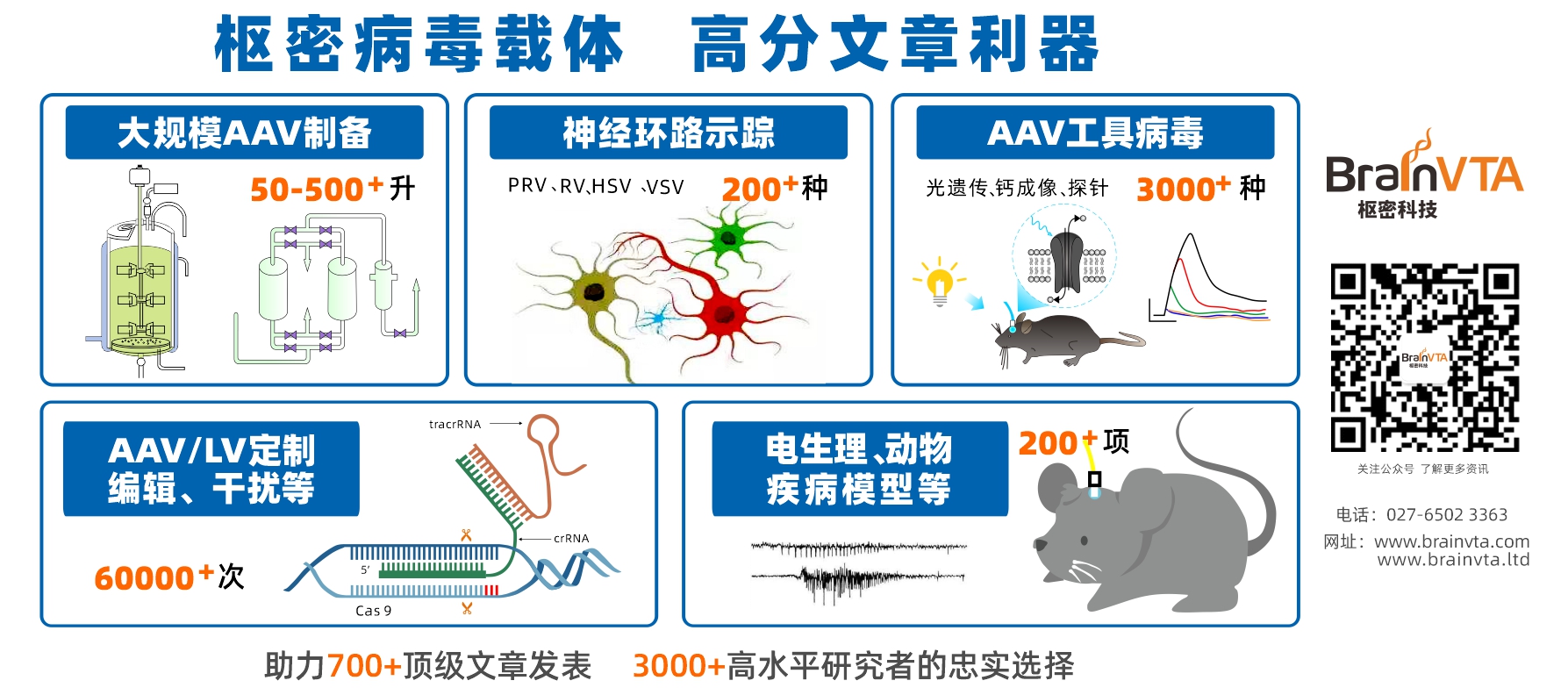
腺相关病毒载体(AAV)在肺脏的研究及应用
2134 人阅读发布时间:2024-03-04 13:28
腺相关病毒(Adeno-associated Virus,AAV)属于细小病毒科(parvoviridae),病毒颗粒无包膜,结构为直径约20nm的正二十面体,是迄今发现的一类结构最简单且无法自主复制的线性单链DNA病毒,对分裂细胞和非分裂细胞均具有感染力。通过人工进化的方法对AAV衣壳蛋白Cap基因进行定向突变改造,可以筛选到具有高转导效率和不同感染特性的AAV载体,极大增加了AAV的应用潜力。
研究中采用的重组腺相关病毒(Recombination adeno-associated virus,rAAV)载体是在非致病的野生型AAV的基础上改造的基因表达载体,具有种类多样、免疫原性低、安全性高、宿主范围广、扩散能力强、体内表达外源基因时间长等特点,已被广泛的应用在动物水平的基因表达、基因操作和基因治疗。
研究表明AAV5、AAV6和AAV9等对肺有较高的趋向性。目前,AAV已经应用于肺囊性纤维化的临床实验中。
rAAV所包含的DNA一般是用外源基因表达元件替换AAV的编码基因,仅保留了病毒复制和包装所需的ITR序列。通过反式补偿Rep基因、Cap基因和辅助病毒功能因子包装产生携带外源DNA的rAAV。rAAV的载体容量是4.7kb,插入外源目的片段大小不超过2.8kb。
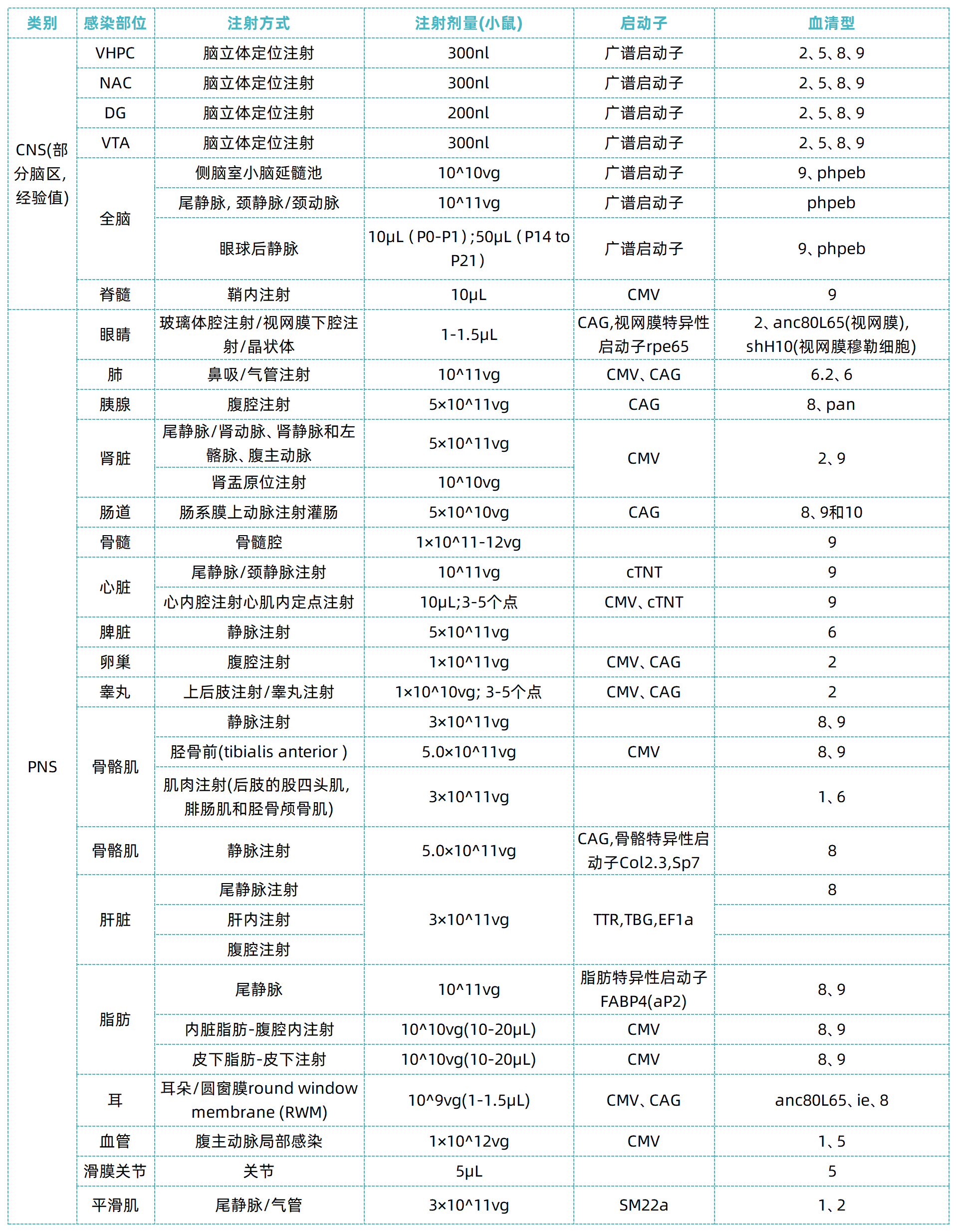
表1.AAV靶向不同的器官及组织推荐使用对应血清型,注射方法及剂量
肺部病毒感染常用的方法有系统注射(尾静脉注射或腹腔注射)、及鼻内或气管内递送(经呼吸道)等。
1)鼻内滴注
鼻内滴注法是一种直接的AAV感染法,操作简单且对设备要求低,对新手友好。但缺点是AAV颗粒容易沉积在上呼吸道(鼻道、鼻窦、咽)和胃肠道,如果需要有效地感染到下呼吸道,则可能需要更大剂量的AAV才能实现。
2)内镜辅助口腔气管插管手术
内镜气管插管术能够将AAV直接灌入肺中,无外科手术风险,且避免了上呼吸道的病毒颗粒损失。由于几乎所有AAV病毒颗粒都会到达肺内,所以要严格控制AAV的使用量。同时,与鼻内滴注法相比,口腔气管插管术需要一些特殊设备,操作起来也稍有难度。
3)气管内注射
与鼻内滴注相比,气管内注射能够提高AAV进入肺部的效率;而与口腔气管插管法相比,设备更简单,操作更容易。但是,气管内注射具有极高的外科手术风险,包括出血、切口开裂、感染以及较长的恢复期等。不仅如此,由于小鼠气管窄小,也很容易出现失误,将AAV注射到气管周围组织或食管中去。
1)

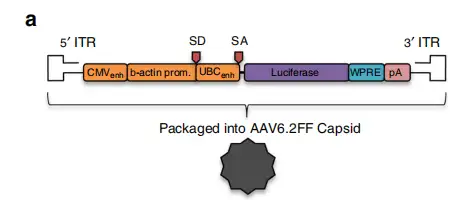
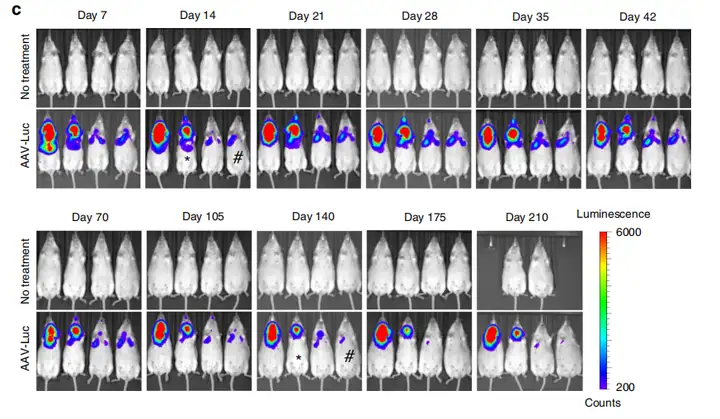
病毒载体为AAV6.2FF-CMVenh(人巨细胞病毒即刻早期基因增强子区)-Luc

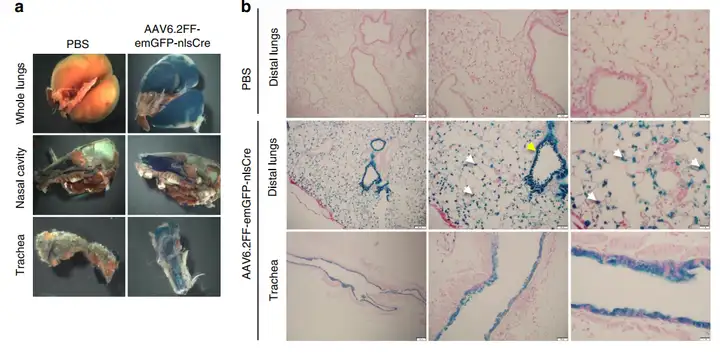
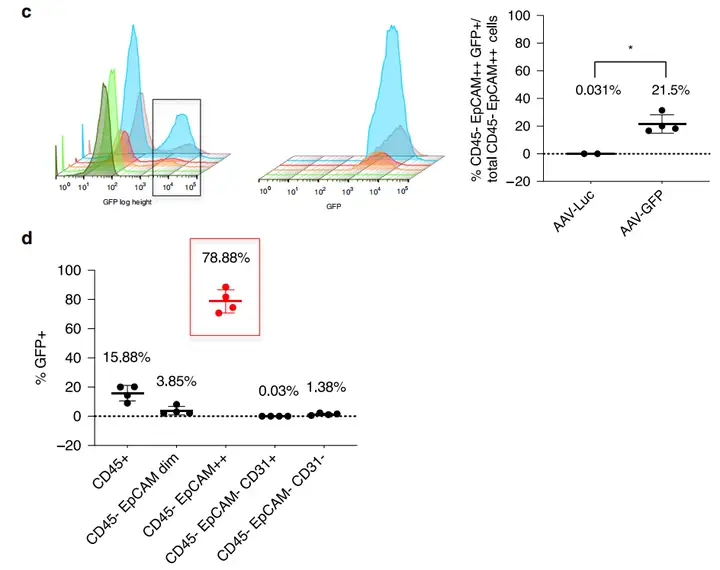
AAV6.2FF-CMV-emGFP-nls-Cre注入Rosa26-Flox/LacZ报告小鼠
参考文献:
Kang MH, van Lieshout LP, Xu L, et al. Nat Commun. 2020.
2)

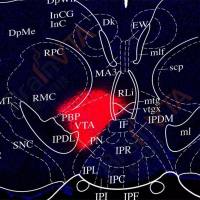
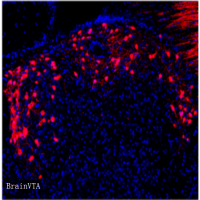
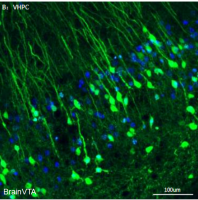
8-10周龄C57BL/6小鼠通过鼻吸导入AAV6-CAG-AP载体,1个月后取肺组织AP染色,结果显示鼻腔上皮细胞、支气管气道上皮细胞、远端气道上皮细胞均被高效转导,且肺的大部分区域几乎所有肺泡细胞也都被染色,从而实现了从鼻腔上皮到远端肺泡的强力转导。
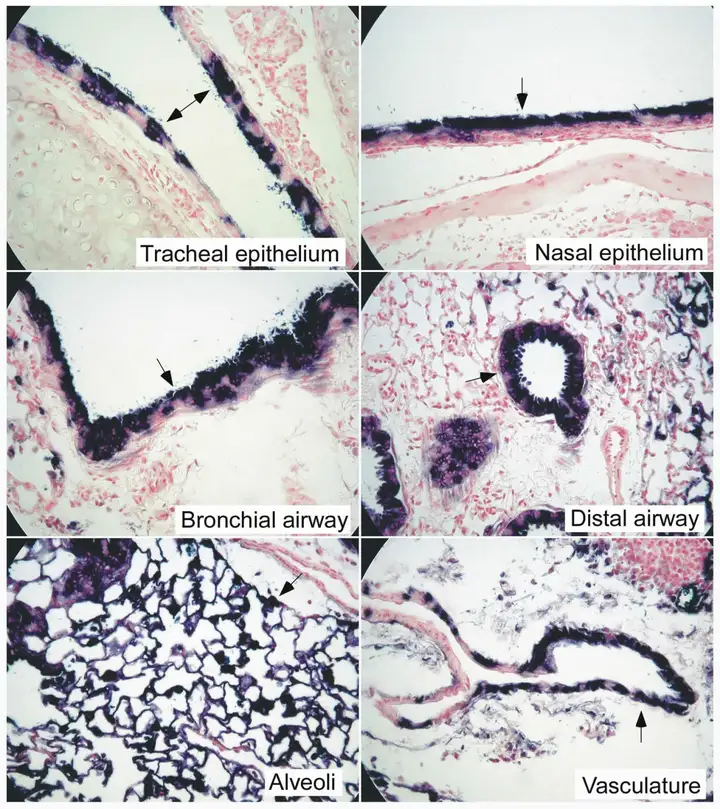
参考文献:
Halbert CL, Lam SL, Miller AD. Hum Gene Ther. 2007.
3)

IL10对博莱霉素诱导肺纤维化的抗炎和抗纤维化作用
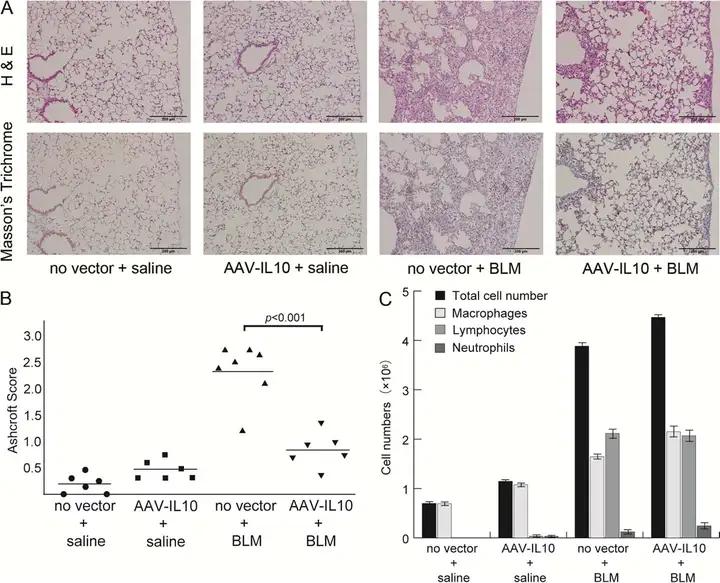
10-12周龄,体重25-30g的雄性C57BL/6J小鼠第0天气管内注射AAV6-CAG-IL10或缓冲液对照,第7天皮下植入渗透微型泵连续一周给125mg/kg博莱霉素(BLM)或生理盐水,小鼠随机分为Group1(无载体+生理盐水)、Group2(IL10过表达+生理盐水)、Group3(无载体+BLM)及Group4(IL10过表达+BLM)4组,并于第35天(BLM处理结束3周后)进行分析。左肺组织切片H&E染色,结果表示Group3中观察到细支气管周围和血管周围有中度至重度炎症浸润,相比之下,Group4中炎性细胞浸润减少,Group1和Group2中都没观察到明显炎症反应。Masson三色染色结果表明Group3小鼠胸膜下区域的肺泡结构破坏和肺间质纤维化,出现明显纤维化变化,同样的Group4小鼠肺纤维化变化减少,且Group1和Group2小鼠肺组织中几乎没观察到纤维化表现。通过Ashcroft纤维化评分进行量化发现AAV6-CAG-IL10的预处理可明显降低评分,即表示能改善BLM诱导的肺部纤维化损伤。
为评估AAV6-CAG-IL10载体对博莱霉素诱导炎症反应的影响,第35天获取小鼠BALF(支气管肺泡灌洗液)并行细胞分析,结果显示Group3和Group4中炎症细胞如巨噬细胞、淋巴细胞和中性粒细胞数量明显比Group1和Group2中多,而AAV6-CAG-IL10的预处理不影响BALF中的炎性细胞。博莱霉素处理小鼠无论是否IL10基因传递,BALF的总细胞数和细胞分类数量是相似的。
参考文献:
Kurosaki F, Uchibori R, Sehara Y,et al.Hum Gene Ther. 2018.
如有相关需求,或了解更多产品服务,欢迎咨询我们!