武汉枢密脑科学技术有限公司品牌商
8 年
手机商铺
- NaN
- 0
- 0
- 1
- 0
武汉枢密脑科学技术有限公司
入驻年限:8 年
- 联系人:
枢先生
- 所在地区:
湖北 武汉市 江夏区
- 业务范围:
抗体、试剂、细胞库 / 细胞培养、技术服务、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 经销商
推荐产品
公司新闻/正文
IF=45.8【客户文章】Science:圣路易斯华盛顿大学团队开发CAR-星形胶质细胞策略,为阿尔茨海默病治疗提供新思路
108 人阅读发布时间:2026-03-24 15:20
近年,针对β-淀粉样蛋白(Aβ)清除的抗体药物为阿尔茨海默病(AD)治疗带来了新的希望,但也暴露出成本、疗效窗口和安全性等方面的现实挑战。首先,这类疗法通常需要较高剂量的抗体,才能实现足够的中枢神经系统(CNS)渗透,因此长期治疗费用十分高昂。其次,目前应用的单克隆抗体(mAb)疗法可能诱发淀粉样相关影像异常(ARIA)等副作用,需对患者进行频繁监测,从而增加了临床实施的复杂性。与此同时,最佳干预窗口的界定仍是一大难题:在疾病早期清除淀粉样沉积,或有望延缓乃至预防AD进展;但若在疾病晚期才启动治疗,则往往难以持续带来显著的认知获益。此外,抗Aβ mAb疗法主要依赖FcRγ信号介导的抗体依赖性细胞吞噬作用(ADCP),这也限制了对细胞反应进行精细调控的灵活性。因此,开发在疗效、安全性、便利性和可调控性方面更具优势的新型AD治疗策略,已成为当前的迫切需求。
2026年3月5日,美国华盛顿大学医学院Marco Colonna教授团队在Science期刊在线发表题为“Targeting amyloid-β pathology by chimeric antigen receptor astrocyte (CAR-A) therapy”的研究论文。该论文的第一作者为陈昀博士,现为Holtzman实验室博士后研究员。在前期抗Aβ治疗研究的基础上,该研究首次将嵌合抗原受体(CAR)技术引入CNS,构建了可在体内长期表达并持续发挥吞噬功能的CAR-星形胶质细胞(CAR-A)。通过对星形胶质细胞进行工程化改造,研究实现了对Aβ的长期、特异性清除。结果显示,该策略不仅显著降低了小鼠脑内的淀粉样负荷,还重塑了脑内胶质细胞生态,提示CAR-A疗法有望成为神经退行性疾病干预的一种全新治疗策略。

Science期刊同期以“Astrocytes engineered to fight Alzheimer’s plaques”为题,对该研究发表了两页篇幅的焦点评论。此后,Science旗下平台Science Adviser又以“Science Adviser: Turning astrocytes against Alzheimer’s”为题进行了进一步报道。随后,国际知名期刊Nature Aging也单独发文对该成果进行了详细介绍。此外,《日本经济新闻》《中国科学报》以及BioArt、丁香园等多个科学媒体和学术传播平台,亦对这项研究成果进行了专题报道。
在本研究中,作者首先在SV40T永生化小鼠星形胶质细胞中验证了CAR在细胞表面的表达及其介导的吞噬功能。随后,又在不同来源的原代星形胶质细胞中进一步评估了四种CAR构建体的功能。鉴于抗体疗效通常依赖于其对纤维状Aβ的优先结合能力,作者进一步比较了来源于Crenezumab和Aducanumab的单链可变片段(scFv)在驱动CAR-A吞噬Aβ方面的效果(图1)。综合比较后,研究团队最终选择了Cre-Megf10和Adu-Dectin1进入后续体内实验。
为实现CAR在体内的稳定表达,作者将相应构建体克隆至由GFAP启动子(星形胶质细胞特异性启动子)驱动的AAV-PHP.eB载体系统中。结果显示,CAR-A可显著增强原代星形胶质细胞对Aβ的摄取能力,其中以Cre-Megf10的效果最为显著。值得注意的是,Adu-Dectin1还可促进小胶质细胞对Aβ的摄取,提示工程化星形胶质细胞可能不仅直接参与Aβ清除,还可能通过分泌因子或细胞表面信号间接调控小胶质细胞功能(图1)。
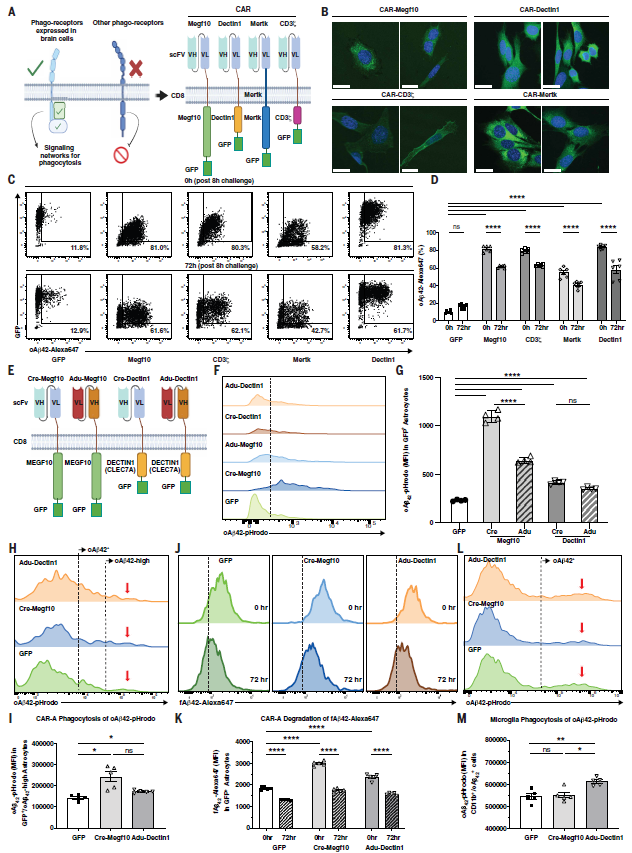
图1. 体外验证CAR-A能帮助星形胶质细胞增加Aβ摄取与降解
之后,作者将构建好的AAV载体注射入6月龄5xFAD小鼠中,单次给药3个月后,淀粉样负荷降低约50%,皮层和海马斑块显著减少,不溶性Aβ42水平下降,同时神经突营养不良明显减轻。Cre-Megf10还部分改善突触丢失(图2)。
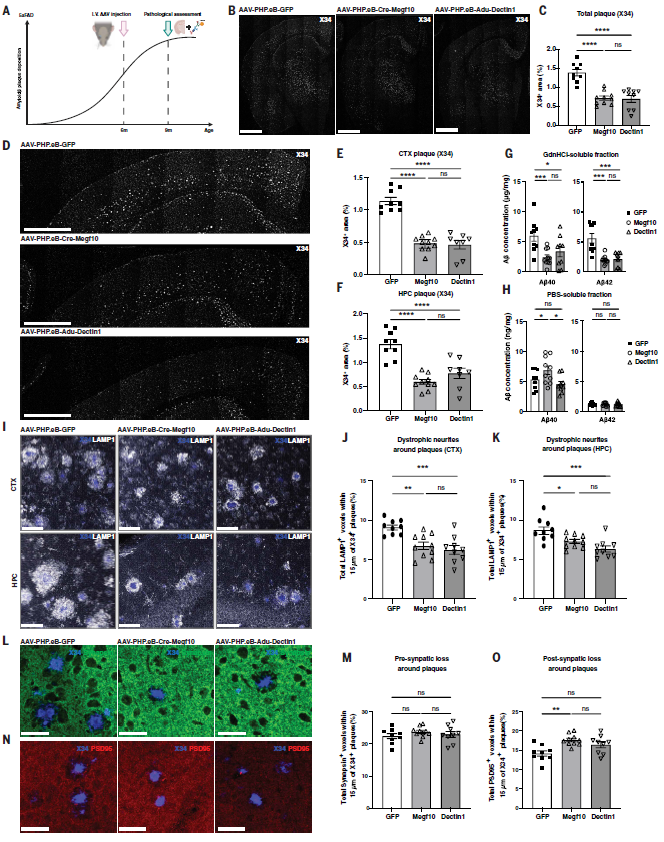
图2. CAR-A在成年5xFAD小鼠中的治疗作用
之前研究表明,某些药物早期干预Aβ沉淀能有效阻止Aβ病理的形成。于是,作者为验证CAR-A的预防性作用,在2.5月龄5xFAD小鼠进行早期给药。结果显示,单针CAR-A治疗可显著抑制斑块形成,其中Cre-Megf10几乎完全阻止Aβ沉积,并减轻神经损伤与突触丢失(图3)。
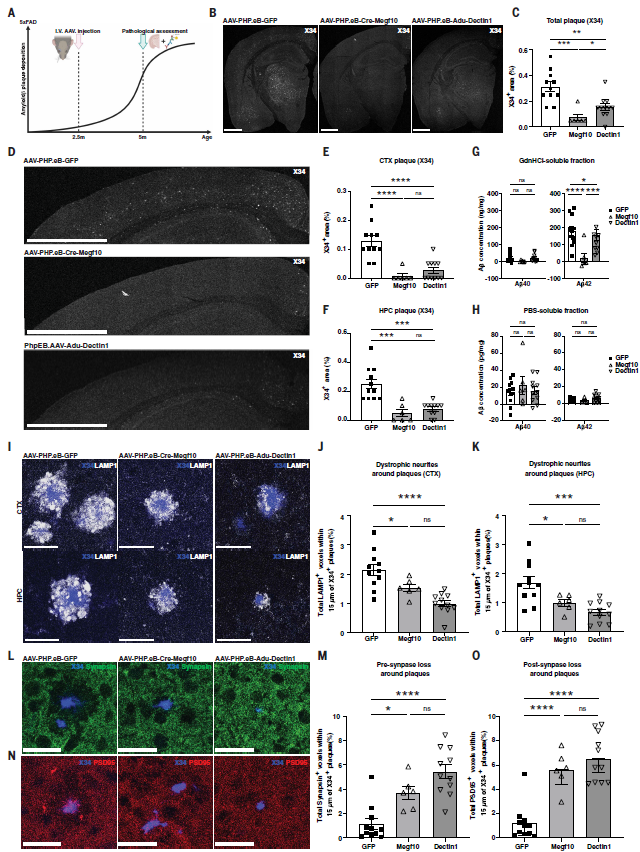
图3. CAR-A在5xFAD小鼠中的预防作用
作者进一步探讨了星形胶质细胞介导的Aβ清除是否会影响斑块周围的胶质反应。结果显示,在9月龄小鼠中,Cre-Megf10可轻度增强星形胶质细胞增生,并促进其向斑块周围聚集;而在5月龄阶段,Adu-Dectin1则更显著地诱导星形胶质细胞增生及围斑块聚集。与此同时,在9月龄小鼠中,Adu-Dectin1还明显增强了小胶质细胞向斑块周围的募集。总体来看,Cre-Megf10更倾向于驱动星形胶质细胞反应,而Adu-Dectin1则更显著促进小胶质细胞聚集(图4)。
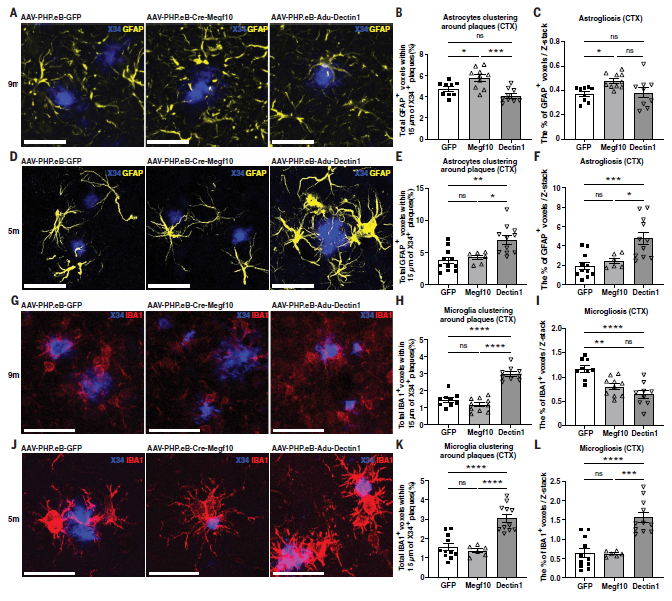
图4. 组织荧光染色显示两种CAR-A治疗导致不同的胶质细胞反应
最后,作者通过单核RNA测序(snRNA-seq)技术证实了AAV在星形胶质细胞中的表达,并发现两种CAR-A均上调与星形胶质发育、神经发生及细胞通讯相关的基因表达,其中Cre-Megf10更显著上调分化及脂质代谢相关通路。在小胶质细胞中,两种CAR-A均上调激活标志基因,而Adu-Dectin1进一步增强主要组织相容性复合体(MHC)相关基因及抗原呈递通路的表达。进一步亚群分析显示,两种CAR-A均扩增疾病相关星形胶质细胞(DAA);但Adu-Dectin1更突出小胶质细胞免疫相关信号通路(图5)。
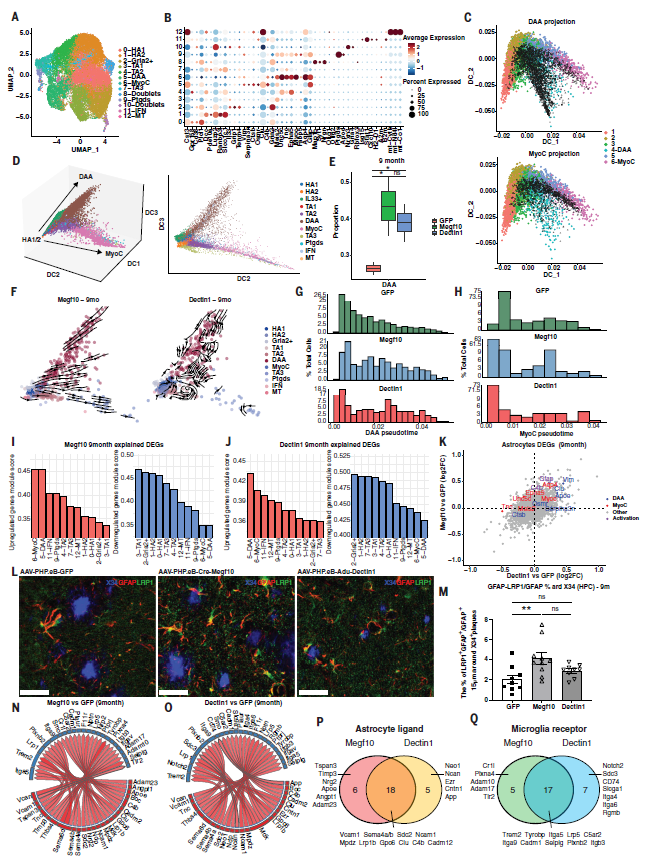
图5. 单细胞核测序验证CAR-A治疗导致的不同星形胶质细胞反应
进一步分析发现,两种CAR-A治疗均诱导形成一个新的小胶质细胞亚群( CSF1Rhigh/CD68high ),并减少经典疾病相关小胶质细胞(DAM)亚群;Adu-Dectin1则额外增加MHC-II阳性小胶质细胞。免疫染色进一步验证,CAR-A治疗后小胶质细胞呈现溶酶体激活状态,同时DAM2标志物表达降低(图6)。总体而言,两种CAR-A不仅促进Aβ清除,还以不同方式重塑胶质细胞状态,这可能反映Aβ负荷下降后小胶质细胞应激水平及耗竭状态的缓解。
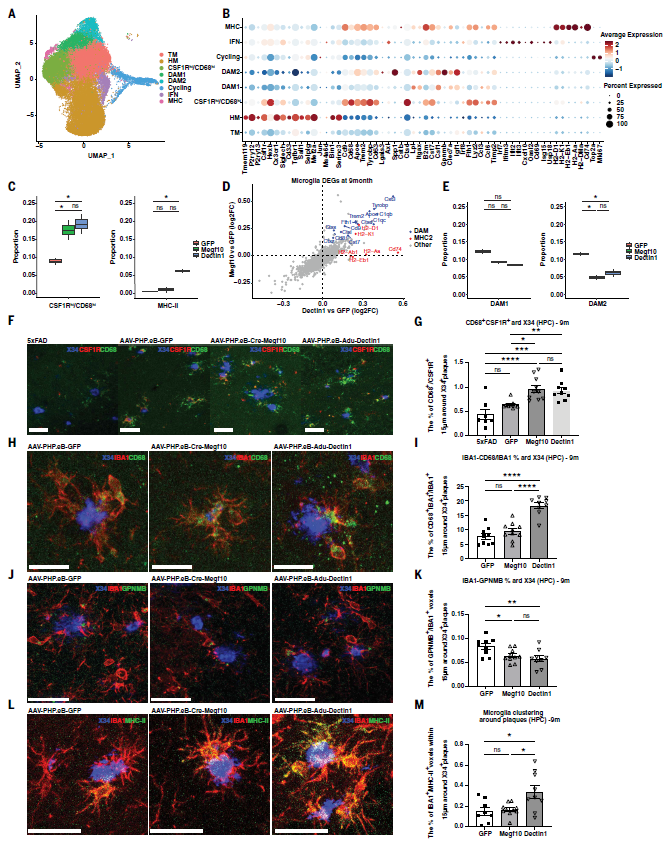
图6. 单细胞核测序验证CAR-A治疗诱发小胶质细胞反应的新类型
结论与讨论
本研究首次提出了嵌合抗原受体星形胶质细胞疗法(CAR-A)的治疗概念。作者通过外周静脉注射AAV-PHP.eB载体,并结合GFAP启动子,实现了两种CAR在脑内星形胶质细胞中的特异性表达,从而显著减轻了小鼠体内的淀粉样病理。在5xFAD小鼠模型中,于Aβ沉积发生前单次给予CAR-A治疗,即可有效阻止淀粉样斑块积累及其相关病理改变。snRNA-seq结果进一步表明,两种CAR-A治疗均可激活星形胶质细胞,并促使小胶质细胞呈现耗竭表型减少的特征;与此同时,不同CAR设计在星形胶质细胞和小胶质细胞的激活模式上又表现出细微差异。
这一策略补充了传统上认为脑内吞噬功能主要由小胶质细胞承担的认知,拓展了神经免疫干预的细胞靶点范围。不同的CAR设计还可驱动部分差异化的胶质细胞程序,凸显了该平台的高度灵活性,以及通过定制CAR信号模块实现特定治疗目标的潜力。未来,这一策略仍有待进一步优化,以在最大.程度增强淀粉样清除效果的同时,更好地保护神经元完整性、降低脱靶效应,并拓展至更多细胞类型和疾病场景。总体而言,该研究将CAR工程确立为一种具有可扩展性和可调控性的神经退行性疾病治疗新策略;随着CAR设计的进一步定向改造,其在小胶质瘤、外周肿瘤以及其他疾病中的应用,也展现出广阔前景。
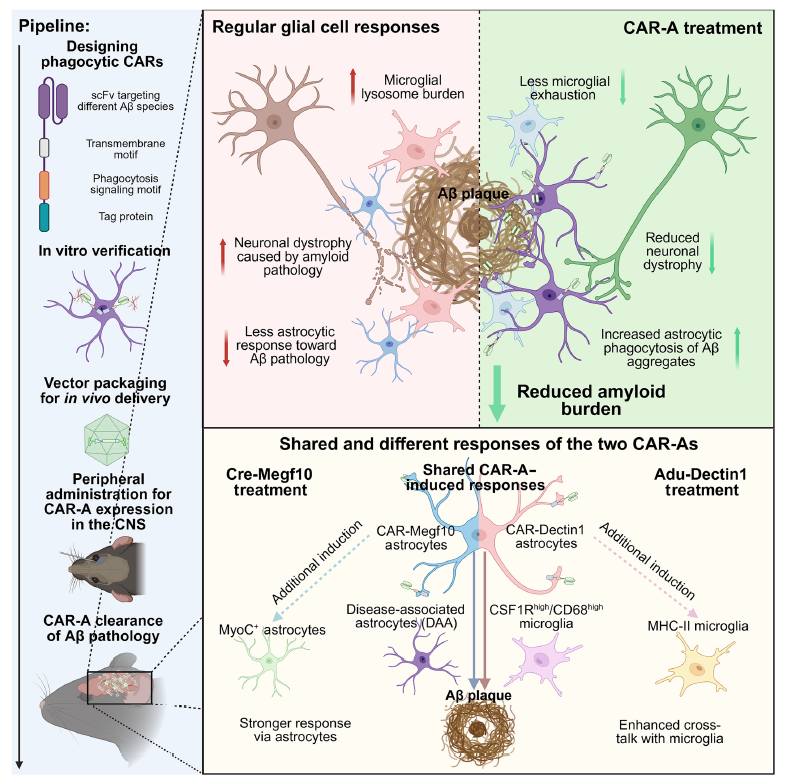
总结图
本文通讯作者为美国圣路易斯华盛顿大学医学院Marco Colonna教授,相关研究亦得到David M. Holtzman教授的重要指导与参与。论文的第一作者为博士后陈昀(现工作于Holtzman实验室,曾是Holtzman和Colonna教授的共同学生),共同第一作者还包括博士学生Yizhou Liu和Khai Nguyen。该项工作获得美国国立卫生研究院(NIH)等机构的资助。相关CAR设计专利由陈昀和Marco Colonna教授享有。
本文使用的AAV.PHPeB病毒载体全部来自枢密科技,相关CAR序列专利属于陈昀和Marco Colonna教授,如有需求请联系Colonna教授。病毒列表如下:

如有相关需求,或了解更多产品服务,欢迎咨询我们!点击进入店铺,查看更多产品及服务