武汉枢密脑科学技术有限公司品牌商
8 年
手机商铺
- NaN
- 0
- 0
- 1
- 0
武汉枢密脑科学技术有限公司
入驻年限:8 年
- 联系人:
枢先生
- 所在地区:
湖北 武汉市 江夏区
- 业务范围:
抗体、试剂、细胞库 / 细胞培养、技术服务、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 经销商
推荐产品
公司新闻/正文
基因沉默:CRISPRi vs. RNAi !CRISPRi和RNAi各有什么特点?
2181 人阅读发布时间:2023-09-08 09:31
Genotype-Phenotype的关联是研究基因功能和相关疾病治疗的基础问题。Loss-of-function (LOF) 实验,通过干扰正常的基因表达后观察相应的表型是解析基因功能的金标准。始于2000年的RNAi和近年来众多实验室普及的CRISPR/Cas9是实现基因沉默的两种主要工具,这里简单介绍。
RNAi是实现基因LOF的有力工具,其作用在转录后水平,通过dsRNA诱发细胞中存在的microRNA机器,破坏互补的mRNA序列来实现敲减;CRISPR/Cas9系统介导的基因沉默依赖于Cas9核酸酶,在sgRNA的指引下对genome DNA切割,细胞自身对DNA的修复过程中引入indels,移码后产生等位基因的功能性敲除。这两种技术介导基因沉默的生物学机制存在根本性差异,导致phenotype的不同。
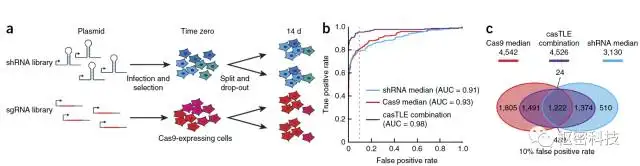
Figure 1. K562 细胞系中平行筛选必需基因[Ref 1]。shRNA介导的敲低存在异质性,CRISPR/Cas9导致的框内indels,WT和杂合子细胞亚群同样干扰筛选结果。上图显示,与RNAi相比,Cas9技术筛选得到的必需基因种类更多。但是,这两种方法鉴定出不同类别的基因。NOTE: K562细胞系源于CML女性病人。
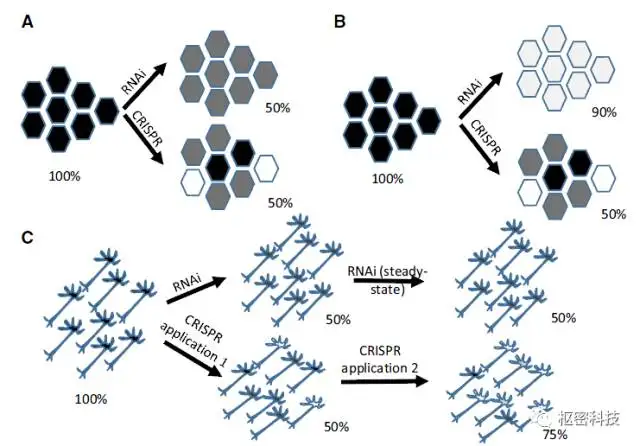
Figure 2. RNAi 和CRISPR/Cas9沉默效率示意[Ref 2]。整体的抑制效率中存在单个细胞差异。
CRISPRi (CRISPR Interference)系统是在CRISPR/Cas9 的基础上发展而来的,可特异性地抑制靶基因的转录而并非将基因knockout来实现调控。相比于knockout,CRISPRi 能够在不同水平对靶基因进行剂量控制的敲减。
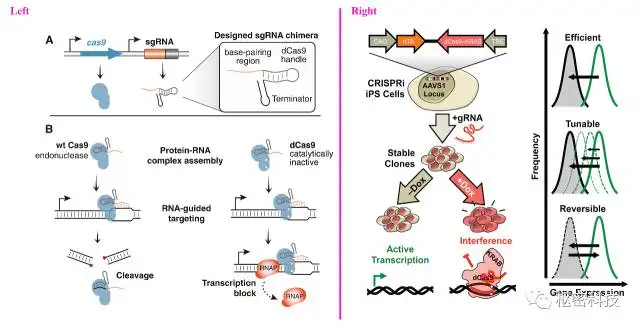
Figure 3. CRISPRi 的工作原理[Ref 3, 4]。dCas9缺少核酸酶的切割活性,与sgRNA形成complex后结合到蛋白编码区,阻断RNA聚合酶和转录本延伸。dCas9与转录抑制子KRAB domain融合,sgRNA-dcas9-KRAB聚合体结合到TSS(转录起始位点),阻断RNAP的转录进程 (Left)。诱导型的TetO CRISPRi系统,通过加入rtTA序列,可以实现DOX药物诱导的CRISPR干扰 (Right)。
虽然RNAi or CRISPRi均用于基因的LOF研究,可互为补充,但作用机制和适用范围不同。RNAi 靶向成熟的mRNA,CRISPRi则是在初始阶段就阻断了转录,不依赖于特殊的RNA产物。对于需要靶向核内转录本的研究,RNAi技术难以实现,可以采用CRISPRi。
RNAi 的特点:
1)相比于基因敲除,RNAi介导的基因沉默可快速敲减,快速实现蛋白产物的减少;
2)靶点预测容易,可以进行各种化学修饰,技术成熟;
3)siRNA可以兼容多种投递方法,如脂质体,纳米载体,病毒载体等;
4)除了目标靶序列,siRNA也会结合到其他mRNA上;
5)siRNA敲减表现出剂量依赖效应,不同程度的敲低可能出现不同的表型;
6)较好的沉默实验中,siRNA可效率可达90-95%,但是最少要实现70%以上的效率。
NOTE:请注意siRNA和shRNA在in vitro和in vivo水平的使用差异。
CRISPRi 的特点:
1)CRISPRi介导的基因下调是高度特异的;
2)相比RNAi,脱靶的发生要低很多并且可以通过优化设计进一步降低脱靶效应;
3)CRISPRi有效干扰转录起始和延伸;
4)CRISPRi介导的敲低是可诱导且可逆的;
5)CRISPRi同时靶向多个基因,实现基因组水平的分析,实现转录网络调控;
6)CRISPRi在哺乳动物和微生物中均可以实现;
7)CRISPRi用于功能基因筛选时,在不同细胞系之间结果更为一致,但不排除高丰度表达或有多个转录本存在,抑制效果不佳的可能;
8)对同一RNA,CRISPRi产生的knockdown表型更为明显。
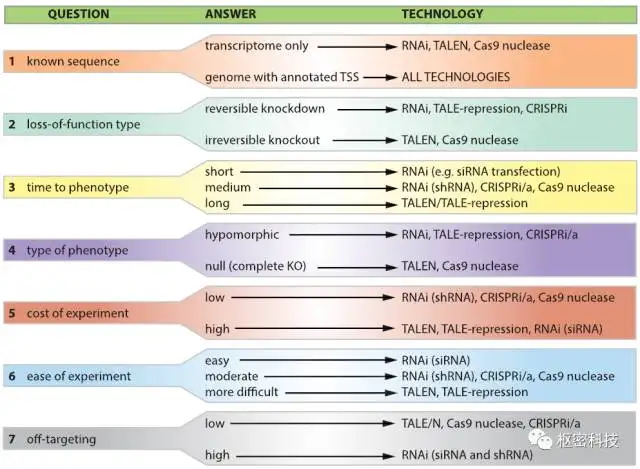
Figure 4. RNAi,TALEN和CRISPR方法的比较[Ref 5]。
尽管更精准的多水平调控的CRISPR新工具和新应用不断涌现,但是RNAi 和CRISPRi 两种方法在使用上各有优势, 在一段时间内二者还是会同时作为基因功能研究的工具使用。
References:
[1]. Nat Biotechnol. 34,634–636 (2016) doi:10.1038/nbt.3567.
Systematic comparison of CRISPR/Cas9 and RNAi screens for essential genes
[2]. FEBS J. 2016 Sep;283(17):3249-60. doi: 10.1111/febs.13742.
Stacking up CRISPR against RNAi for therapeutic gene inhibition.
[3]. Cell. 2013 Feb 28; 152(5): 1173–1183. doi: 10.1016/j.cell.2013.02.022
Repurposing CRISPR as an RNA-Guided Platform for Sequence-Specific Control of Gene Expression.
[4]. Cell Stem Cell. 2016. April 7. p541–553.DOI: http://dx.doi.org/10.1016/j.stem.2016.01.022
CRISPR Interference Efficiently Induces Specific and Reversible Gene Silencing in Human iPSCs.
[5]. Mol Cell. 2015 May 21;58(4):575-85. doi: 10.1016/j.molcel.2015.04.028.
Choosing the Right Tool for the Job: RNAi, TALEN, or CRISPR.
如有相关实验需求,或了解更多产品服务的详情与报价,欢迎咨询我们!
点击进入店铺,查看更多产品和服务