武汉枢密脑科学技术有限公司品牌商
8 年
手机商铺
- NaN
- 0
- 0
- 1
- 0
武汉枢密脑科学技术有限公司
入驻年限:8 年
- 联系人:
枢先生
- 所在地区:
湖北 武汉市 江夏区
- 业务范围:
抗体、试剂、细胞库 / 细胞培养、技术服务、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 经销商
推荐产品
公司新闻/正文
枢密客户文章精读:觉醒调控—丘脑室旁核是重要的丘脑觉醒调控核团
1102 人阅读发布时间:2023-08-04 11:21
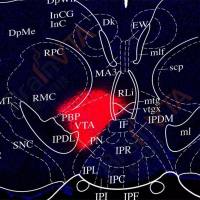
人的一生中有1/3的时间处于睡眠状态,那么,剩下的2/3的时间在做什么呢?当然是处于觉醒状态。我们在觉醒期间参与摄食、运动、认知和社交等活动。由此可见,觉醒对生命活动是必不可少的。临床研究发现,动脉梗塞所致的旁正中丘脑卒中病人表现出不同程度的意识障碍症状,包括嗜睡甚至昏迷。这些研究提示旁正中丘脑是重要的丘脑觉醒调控位点。旁正中丘脑包含许多不同的神经元核团,如丘脑室旁核、连接核、背内侧核和前内侧核等。这些旁正中丘脑核团具有不同的输入输出联系,同时参与不同的脑功能。但是,参与觉醒调控的旁正中丘脑核团及其相关神经环路尚未鉴定。
2018年10月26日,《SCIENCE》杂志(2017年-2018年影响因子41.058)发表陆军军医大学基础医学院生理学教研室/脑科学协同创新中心胡志安教授课题组题为“The paraventricular thalamus is a critical thalamic area for wakefulness”的研究论文,该论文回答了上述问题。论文中利用多通道电生理记录技术、脑电-肌电记录技术、光纤记录技术、化学遗传学、光遗传学和免疫组织化学技术证实丘脑室旁核(paraventricular thalamus, PVT)是参与维持觉醒的关键脑区。同时,通过病毒示踪技术、环路特异性化学遗传学、光遗传学和离体、在体电生理记录技术等方法从解剖和功能学层次鉴定PVT调控觉醒的上下游神经环路联系。该研究工作得到了国家自然科学基金等项目的资助。

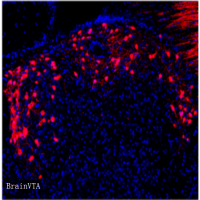
作者首先观察旁正中丘脑在不同睡眠-觉醒状态下的cfos表达谱,发现PVT在觉醒或延长觉醒状态下,表现出最高水平的cfos表达(fig. S1)。为进一步研究PVT神经元在睡眠-觉醒周期中的活动模式,作者采用多通道电生理记录技术,发现PVT在觉醒状态下放电频率最高(Fig1. A-C)。PVT神经元放电频率在由觉醒向睡眠转换过程中逐渐下降;反之,在睡眠向觉醒转换过程中,PVT神经元放电频率急剧增高。通过向PVT注射AAV-CaMKIIα-hM4D-mCherry,作者发现化学遗传学抑制PVT谷氨酸能神经元能明显降低觉醒(Fig1. G-I)。此外,采用兴奋性毒性毁损或白喉毒素特异性杀死PVT神经元,能显著降低黑暗期觉醒水平,并引起脑电能谱变化(Fig1. J-L and fig. S10)。
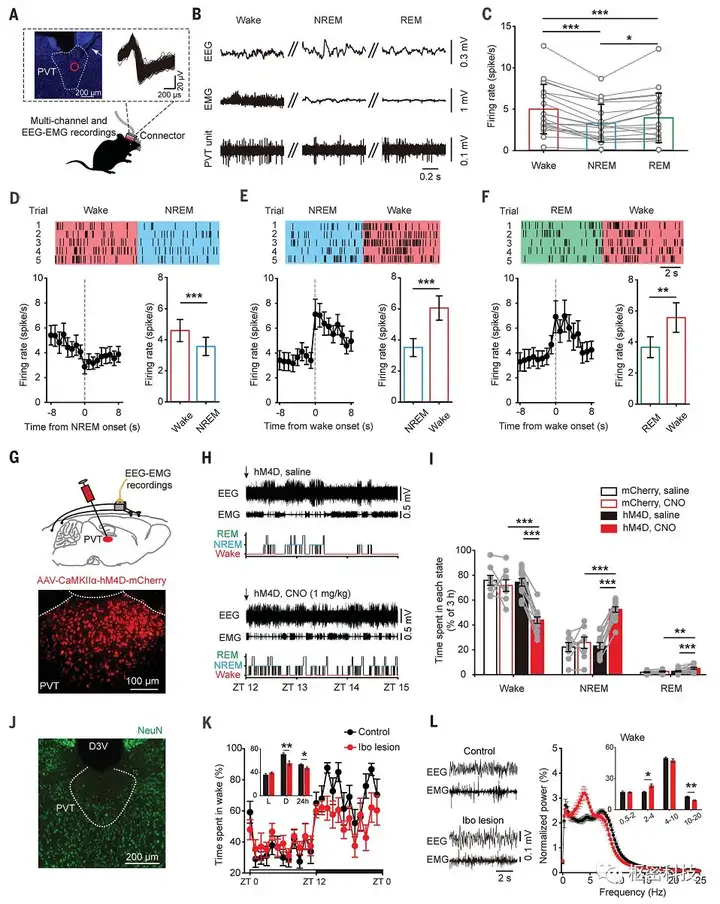
Fig. 1. PVT glutamatergic neurons are required for the control of wakefulness
为进一步验证PVT对觉醒维持的充分性,作者采用光遗传方法激活PVT谷氨酸能神经元。作者在PVT注射AAV-CaMKIIα-ChR2-mCherry,并通过膜片钳技术验证其功能性表达(Fig2. A and B)。作者发现,在非快眼动睡眠(NREM)期激活PVT谷氨酸能神经元诱发刺激频率依赖性的睡眠向觉醒转换,同时增加觉醒概率,降低睡眠概率(Fig2. C-E)。为进一步研究激活PVT是否能够诱导由无意识状态向觉醒的转换,作者接下来在麻醉状态下激活PVT谷氨酸能神经元。在无意识(异氟烷诱导麻醉)状态下,激活PVT增加皮层burst放电,表现为burst时程的增长及burst抑制比例下降,提示皮层神经元的激活。更为重要的是,持续激活PVT显著加速小鼠由麻醉向觉醒状态恢复所需的时间(Fig2. F-K)。
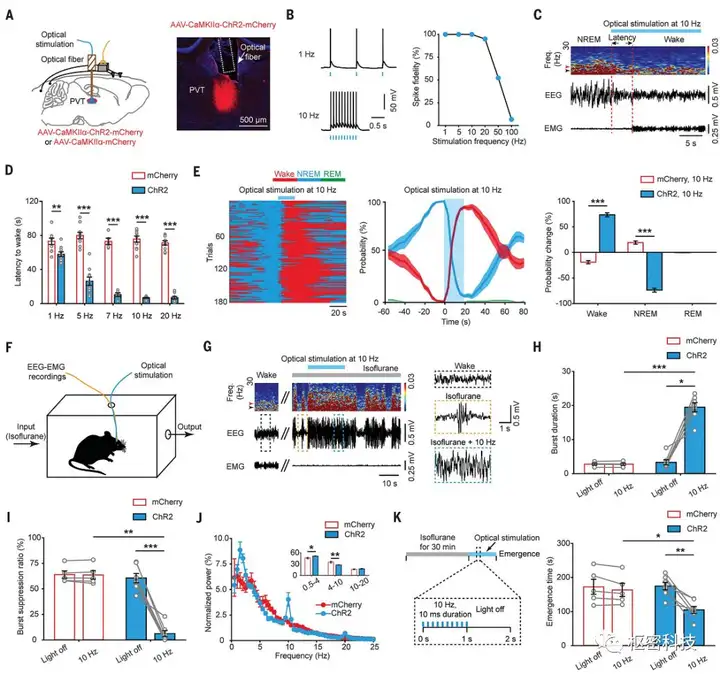
Fig. 2. Optogenetic activation of PVT glutamatergic neurons induces wakefulness from sleep and general anesthesia.
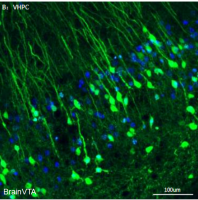
上述研究证明PVT对觉醒调控具有必要性和充分性。作者就PVT发挥觉醒调控作用的下游神经环路机制展开进一步研究。通过AAV-CaMKIIα- ChR2-mCherry介导的顺行环路示踪技术,作者发现PVT谷氨酸能神经元投射至多个皮层及皮层下脑区,如内侧前额叶皮层、岛叶皮层以及参与觉醒调控的伏隔核(nucleus accumbans, NAc)等。直接激活PVT→皮层通路不能诱发睡眠向觉醒的转化(Fig3. A-C),提示PVT→皮层通路不参与觉醒的调控。但是,作者发现激活PVT→NAc通路能够诱发快速的睡眠-觉醒转换(Fig3. D and E)。光遗传学激活NAc内的PVT末梢,能够快速诱发EPSC,证实PVT谷氨酸能神经元与NAc神经元之间形成功能性单突触联系(Fig3. F)。此外,作者在NAc注射逆行Cre病毒(AAVretro-Syn-Cre),同时在PVT注射Cre依赖性AAV-DIO-hM4D-mCherry,由此采用化学遗传学方法抑制NAc投射-PVT神经元(Fig3. G)。作者发现抑制NAc投射-PVT神经元能显著降低觉醒量(Fig3. H and I),从而证明PVT谷氨酸能神经元通过PVT→NAc环路调控觉醒。
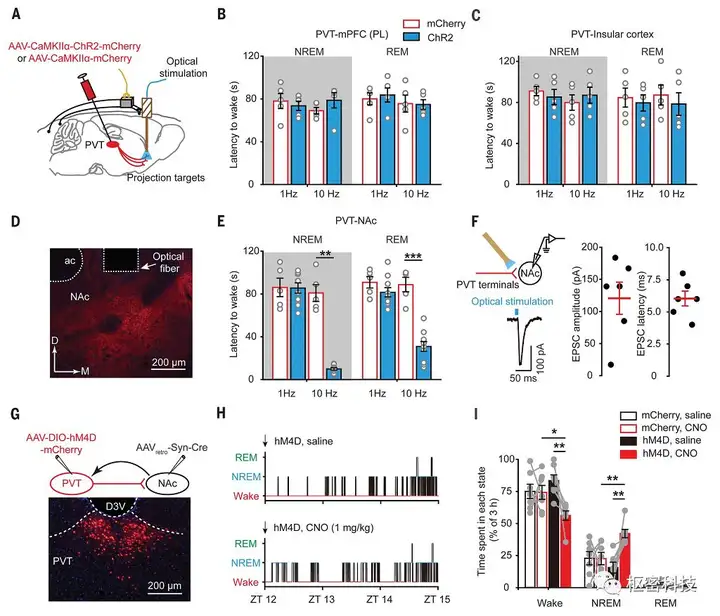
Fig. 3. PVT glutamatergic neurons control wakefulness through the PVT-NAc pathway.
前述研究证明PVT发挥觉醒调控作用的神经环路机制,但是PVT的活动接受来自何种神经元输入的调节呢?为回答这一问题,作者采用基于狂犬病毒的逆行单突触示踪技术,在vGlut2-Cre小鼠中研究PVT谷氨酸能神经元上游输入神经元的分布。作者发现, PVT谷氨酸能神经元接受大量来自外侧下丘脑(LH)食欲肽神经元(hypocretin, Hcrt)的输入(figS19)。为了从功能学角度验证LHHcrt→PVT环路在觉醒调控中的作用,作者首先在Hcrt-Cre小鼠中采用化学遗传学方法抑制LHHcrt→PVT环路。作者发现,PVT局部应用CNO显著降低觉醒量(Fig4. A-C)。接着,作者在Hcrt-Cre小鼠PVT埋置光电极,采用光遗传学方法激活LHHcrt→PVT环路。激活PVT内Hcrt神经元末梢显著增加PVT神经元放电频率,并诱发睡眠向觉醒的转换(Fig4. D-G)。这一效应能够被Hcrt受体阻断剂TCS-OX 2-29部分阻断(Fig4. H)。上述结果表明,PVT的觉醒调控功能受到外侧下丘脑食欲肽神经元的调节。
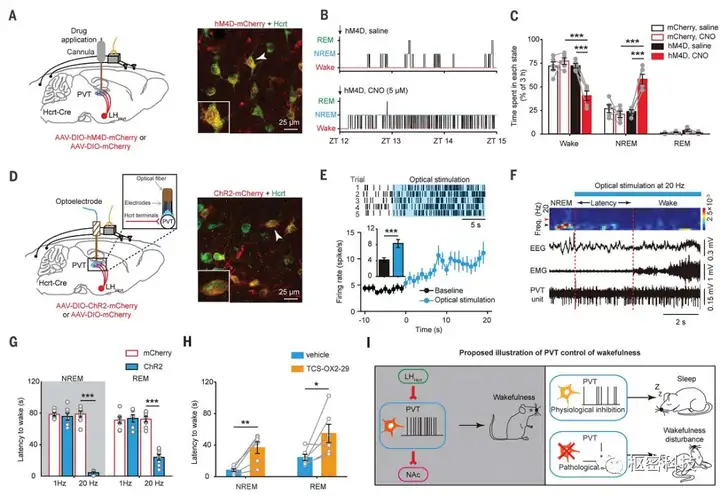
Fig. 4. The wakefulness-controlling function of the PVT is regulated by Hcrt neurons.



文章中使用的来自枢密科技的病毒工具
如有相关实验需求,或了解其他产品和服务,欢迎咨询我们!