武汉枢密脑科学技术有限公司品牌商
8 年
手机商铺
- NaN
- 0
- 0
- 1
- 0
武汉枢密脑科学技术有限公司
入驻年限:8 年
- 联系人:
枢先生
- 所在地区:
湖北 武汉市 江夏区
- 业务范围:
抗体、试剂、细胞库 / 细胞培养、技术服务、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 经销商
推荐产品
公司新闻/正文
【文献解读】Nature Communications丨BNST相关微通路参与炎症介导的摄食调控
1576 人阅读发布时间:2023-06-14 11:03
食欲减退或与炎症有关的厌食症严重损害了人们的身体健康,并增加许多疾病的发病率,炎症相关的食欲下降或厌食症是影响众多疾病中患者生活质量和病程转归的重要因素,然而,介导炎症性厌食症的确切神经机制仍知之甚少【1-3】。在不同脑区,尤其是弓状核(the arcuate nucleus, ARC)、外侧旁核(lateral parabrachial nucleus, LPB)、杏仁中央核(central nucleus of amygdala, CEA) 和终纹床核(bed nucleus of stria terminalis, BNST)【4-8】,其中许多与摄食的调节密切相关。然而,除了LPB神经元在LPS【9】引起的厌食中起到了温和的调节作用外,目前为止,ARC和CEA中的神经元对炎症相关的厌食症没有调节作用。例如,激活ARC AGRP(Agouti-related protein)神经元可以有效地促进摄食,但不能恢复LPS诱导的厌食【10】。沉默CEA神经元的一个特定亚群可以阻断由不同厌食信号引起的厌食症,但不能挽救由LPS引起的厌食【11】。
与ARC、LPB和CEA神经元相比,BNST神经元在摄食中的作用尚不清楚。最近的一些研究表明,BNST神经元可能在调节摄食中起作用。ARC AGRP神经元或结节核(tuberalnucleus, TN)生长抑素神经元投射激活BNST中抑制的γ-氨基丁.酸(GABA能)神经末梢促进了摄食【12-14】。光激活由VGAT(vesicular GABA transporter, VGAT)标记的BNST神经元到外侧下丘脑(lateral hypothalamus, LH)这条重要的摄食神经通路,也能诱导摄食【15】。此外,在BNST的药理学研究以及解剖学研究中也表明,BNST亚区的神经元在应激或其他条件下的摄食调节中可能发挥特定的作用【16-18】。然而,BNST中的神经元是否真的调节摄食或在炎症相关的厌食症中发挥作用,以及哪种类型的BNST神经元参与调节尚不清楚.
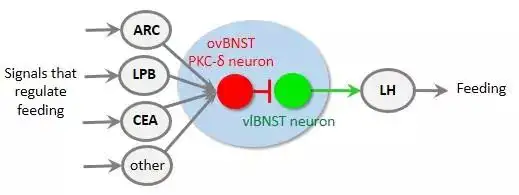
2019年6月24日,来自亚利桑那大学Dr. Haijiang Cai和西安交大医学部王勇副教授的研究团队在《Nature Communications》上在线发表了题为“A bed nucleus of stria terminalis microcircuit regulating inflammation-associated modulation of feeding”的研究论文。本研究以野生型和PKC-δ-Cre的C57BL/6小鼠为研究对象,使用光遗传学和化学遗传学等多种实验技术,发现椭圆部BNST(ovBNST)内的PKC-δ+神经元参与动物炎症引起的厌食症状,并对正常动物的摄食行为发挥双向调控作用。ovBNST内的PKC-δ+神经元接受ARC、LPB和CEA等多个摄食相关脑区的传入调控,并对腹外侧BNST(vlBNST)内对摄食活动有重要作用的LH投射神经元的活动发挥抑制性调节作用。结果显示,BNST内的PKC-δ+神经元群及相关神经通路是参与炎症相关摄食调控的关键脑区。

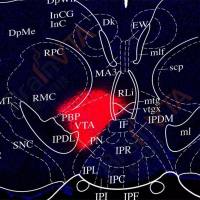
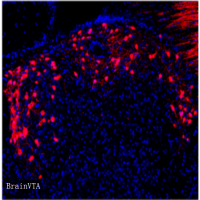
研究首先发现,ovBNST内的PKC-δ+神经元参与 IL-1β和LPS相关的厌食症状调控。腹腔注射IL-1β或LPS可以增加BNST内神经元的c-Fos表达,其中约80%的c-Fos阳性表达神经元为PKC-δ+神经元。为证明ovBNST内PKC-δ+神经元是否直接参与炎症相关厌食症状调节,研究者将Cre依赖的AAV-hM4Di或AAV-mCherry病毒注入PKC-δ-Cre小鼠的双侧ovBNST。病毒注射后4w,观察注射CNO对IL-1β或LPS相关厌食症状的影响。结果显示,与对照组比较,注射CNO抑制PKC-δ+神经元活动可显著减轻IL-1β或LPS注射后的厌食症状。离体脑片电生理实验也显示,CNO可以显著抑制表达hM4Di神经元的电活动。
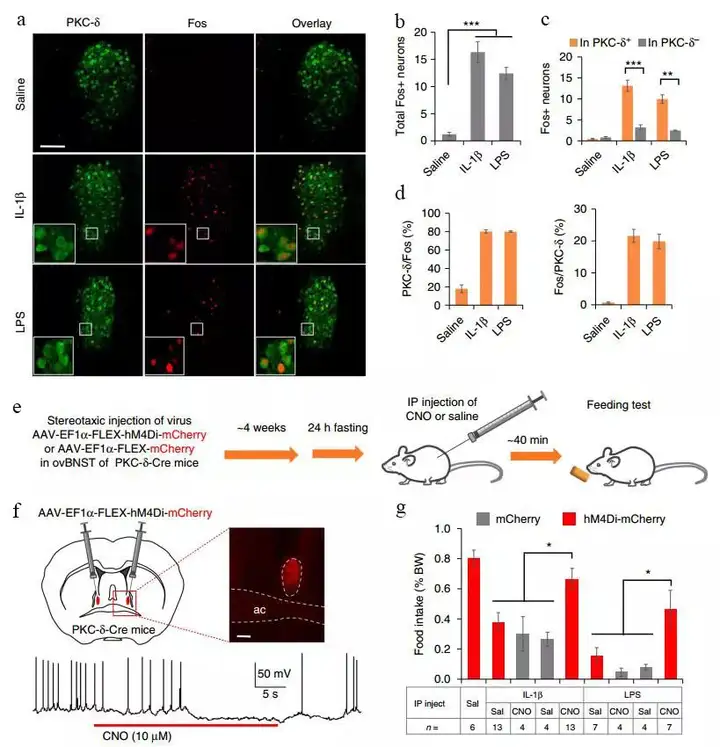
图1. ovBNST内的PKC-δ+神经元参与 IL-1β和LPS相关的厌食症状调控
为了进一步阐明ovBNST PKC-δ+神经元在摄食调控中的作用,研究者将Cre依赖的AAV-ChR2病毒注射入PKC-δ-Cre小鼠的双侧ovBNST,并在注射部位之上埋置光纤。结果显示,473nm光刺激ovBNST PKC-δ+神经元可显著抑制正常和禁食24h小鼠的短期摄食行为,对动物的运动、焦虑水平等无显著影响。用化学遗传学方法(hM3Dq-CNO)刺激ovBNST PKC-δ+神经元则可以在长达2h的实验中显著抑制动物的摄食。与此相反,化学遗传学方法(hM4Di-CNO)抑制ovBNST PKC-δ+神经元可显著促进正常和禁食24h小鼠的摄食行为,增加进食量和进食时间。这些结果显示,ovBNST PKC-δ+神经元可双向调控正常状态动物的摄食行为。
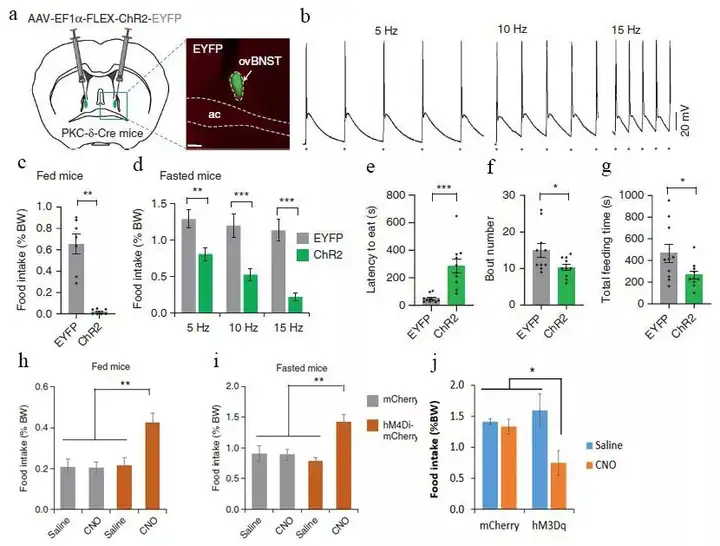
图2. ovBNST PKC-δ+神经元可双向调控动物的摄食行为
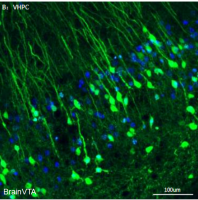
为阐明ovBNST PKC-δ+神经元参与摄食调控的神经机制,研究者开展PKC-δ-Cre小鼠ovBNST内Cre依赖AAV-ChR2病毒注射后的离体脑片电生理实验。结果显示,ovBNST PKC-δ+神经元对vlBNST的PKC-δ-神经元有直接的抑制性投射。光刺激ovBNST PKC-δ+神经元,可在vlBNST记录到单突触的IPSC。为证明vlBNST的PKC-δ-神经元是否参与摄食调节,研究者将AAV-Flp和AAV-FlpON/CreOFF-ChR2注射入PKC-δ-Cre小鼠的vlBNST并埋置光纤。行为学实验结果显示,光刺激vlBNST的PKC-δ-神经元显著促进动物的摄食行为,这与光刺激ovBNST PKC-δ+神经元的作用正好相反。顺向束路追踪的结果显示,vlBNST的PKC-δ-神经元主要投射至LH。为检测vlBNST-LH投射纤维是否参与摄食调节,研究者将ChR2表达于vlBNST的PKC-δ-神经元,将刺激光纤埋置在LH上方。结果显示,光刺激vlBNST-LH投射纤维显著促进动物的摄食行为,而用化学遗传学方法抑制vlBNST-LH投射神经元则对动物的摄食有抑制作用。这部分结果显示,vlBNST的LH投射神经元在摄食调节中发挥与ovBNST PKC-δ+神经元不同的作用。
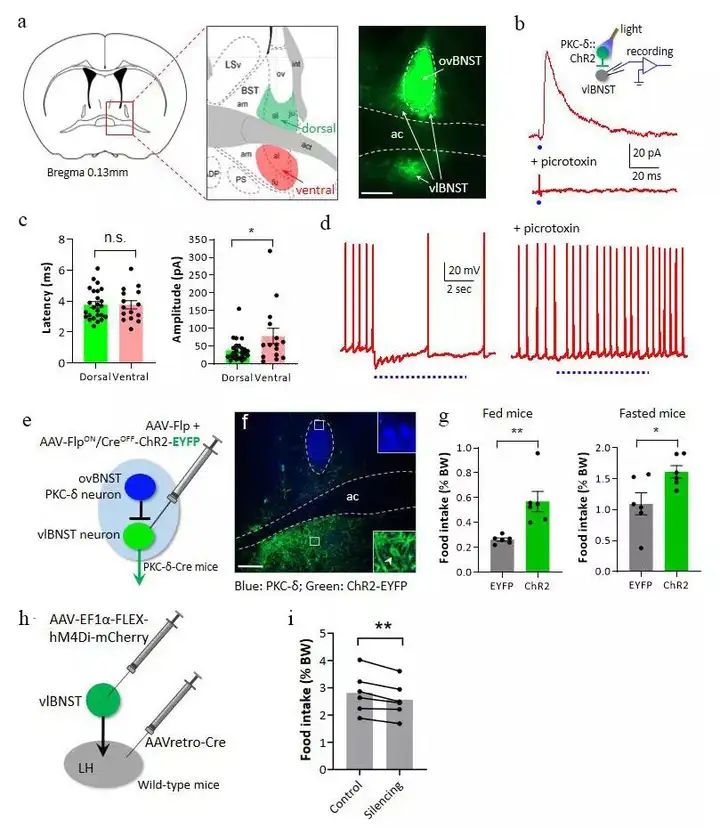
图3. vlBNST的LH投射神经元在摄食调节中发挥与ovBNST PKC-δ+神经元不同的作用
为更深入阐明参与摄食调节的vlBNST的PKC-δ--LH投射神经元和ovBNST PKC-δ+神经元之间的功能联系,研究者用LH内CTB注射的方法标记了vlBNST的LH投射神经元, 通过离体脑片电生理记录观察光刺激PKC-δ+神经元对vlBNST内CTB标记神经元活动的影响。光刺激ovBNST PKC-δ+神经元,可在vlBNST内CTB标记神经元上记录到单突触IPSC。为验证vlBNST的PKC-δ--LH投射神经元和ovBNST PKC-δ+神经元之间的解剖联系,研究者将AAVretro-Cre注射入野生型小鼠的LH,将Cre依赖的AAV-hSyn-FLEX-TVA-P2A-eGFP-2A-oG注射入vlBNST。这样vlBNST内的LH投射神经元会表达eGFP、TVA和oG。在vlBNST内进一步注射G-deleted rabies-dsRed病毒后,对vlBNST-LH神经元有单突触投射的上游神经元将表达dsRed。结果显示,BNST内的LH投射神经元多为vlBNST内的PKC-δ-神经元,而其上游的dsRed阳性神经元大部分为PKC-δ+神经元。研究者进一步将ChR2同时表达于ovBNST PKC-δ+神经元和vlBNST内的LH投射神经元,结果显示,同时光刺激vlBNST-LH投射神经元可以反转光刺激ovBNST PKC-δ+神经元引发的摄食抑制行为。这些结果,进一步证明ovBNST PKC-δ+神经元通过对vlBNST-LH投射神经元的直接抑制性投射发挥对动物摄食行为的调节作用。
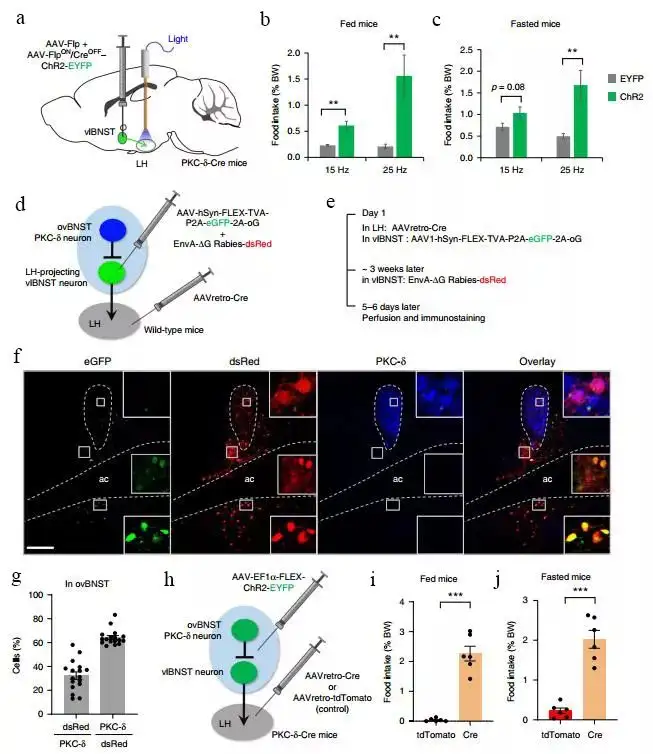
图4. ovBNST PKC-δ+神经元通过对vlBNST-LH投射神经元的直接抑制性投射发挥对动物摄食行为的调节作用
为阐明ovBNST PKC-δ+神经元与摄食相关其他脑区的投射联系,研究者进行了基于Cre依赖的G-deleted rabies-dsRed病毒的逆向束路追踪实验。结果显示,ovBNST内PKC-δ+神经元接受众多脑区的直接传入投射,其中与摄食调节密切相关的ARC、LPB、CEA和TN神经元都对ovBNST内PKC-δ+神经元有直接投射。
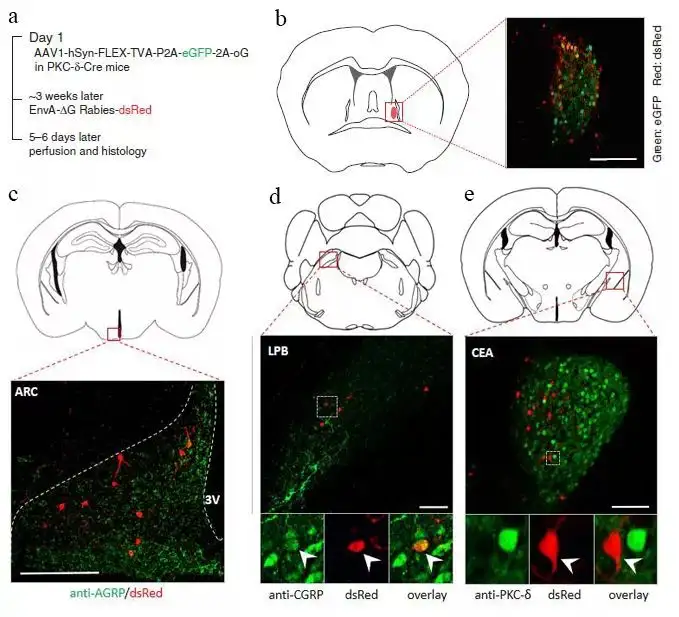
图5. BNST内的PKC-δ+神经元接受ARC、LPB和CEA等多个摄食相关脑区的传入调控
综上所述,本实验中,研究者发现众多炎症因子可以选择性激活位于ovBNST的一群PKC-δ+神经元,使用化学遗传学方法选择性抑制这群PKC-δ+神经元则可抑制炎症相关厌食症状的出现。选择性兴奋或抑制ovBNST内PKC-δ+神经元可双向调控正常状态小鼠的摄食行为。进一步的实验显示,ovBNST内的这群PKC-δ+神经元接受ARC、LPB和CEA等多个摄食调控相关脑区的传入投射,并通过发出抑制性纤维调控vlBNST向LH区投射的神经元的活动进而参与调节动物的摄食行为。
本研究发现和揭示了一条BNST PKC-δ+神经元相关的摄食调控神经微通路。该通路在炎症相关的厌食症状中发挥关键作用,并调控动物的正常摄食行为,可能成为摄食相关疾病治疗干预的新靶点。
西安交通大学王勇副教授为该论文第一作者,美国亚利桑那大学Dr. Haijiang Cai为该论文通讯作者。
参考文献
1. Plata-Salaman, C. R. Anorexia during acute and chronic disease. Nutrition 12, 69–78 (1996).
2. Baracos, V. E., Martin, L., Korc, M., Guttridge, D. C. & Fearon, K. C. H. Cancer-associated cachexia. Nat. Rev. Dis. Primers 4, 17105 (2018).
3. Sternson, S. M. & Eiselt, A. K. Three pillars for the neural control of appetite. Annu. Rev. Physiol. 79, 401–423 (2017).
4. Day, H. E., Curran, E. J., Watson, S. J. Jr. & Akil, H. Distinct neurochemical populations in the rat central nucleus of the amygdala and bed nucleus of the stria terminalis: evidence for their selective activation by interleukin-1beta. J. Comp. Neurol. 413, 113–128 (1999).
5. Elmquist, J. K., Scammell, T. E., Jacobson, C. D. & Saper, C. B. Distribution of Fos-like immunoreactivity in the rat brain following intravenous lipopolysaccharide administration. J. Comp. Neurol. 371, 85–103 (1996).
6. Francesconi, W. et al. The proinflammatory cytokine interleukin 18 regulates feeding by acting on the bed nucleus of the stria terminalis. J. Neurosci. 36, 5170–5180 (2016).
7. Campos, C. A. et al. Cancer-induced anorexia and malaise are mediated by CGRP neurons in the parabrachial nucleus. Nat. Neurosci. 20, 934–942 (2017).
8. Reyes, T. M. & Sawchenko, P. E. Involvement of the arcuate nucleus of the hypothalamus in interleukin-1-induced anorexia. J. Neurosci. 22, 5091–5099 (2002).
9. Carter, M. E., Soden, M. E., Zweifel, L. S. & Palmiter, R. D. Genetic identification of a neural circuit that suppresses appetite. Nature 503, 111–114 (2013).
10. Essner, R. A. et al. AgRP neurons can increase food intake during conditions of appetite suppression and inhibit anorexigenic parabrachial neurons. J. Neurosci. 37, 8678–8687 (2017).
11. Cai, H., Haubensak, W., Anthony, T. E. & Anderson, D. J. Central amygdala PKC-delta(+) neurons mediate the influence of multiple anorexigenic signals. Nat. Neurosci. 17, 1240–1248 (2014).
12. Luo, S. X. et al. Regulation of feeding by somatostatin neurons in the tuberal nucleus. Science 361, 76–81 (2018).
13. Betley, J. N., Cao, Z. F., Ritola, K. D. & Sternson, S. M. Parallel, redundant circuit organization for homeostatic control of feeding behavior. Cell 155, 1337–1350 (2013).
14. Chen, Y. M., Lin, Y. C., Zimmerman, C. A., Essner, R. A. & Knight, Z. A. Hunger neurons drive feeding through a sustained, positive reinforcement signal. eLife 5, e18640 (2016).
15. Jennings, J. H., Rizzi, G., Stamatakis, A. M., Ung, R. L. & Stuber, G. D. The inhibitory circuit architecture of the lateral hypothalamus orchestrates feeding. Science 341, 1517–1521 (2013).
16. Williams, D. L. et al. GLP-1 action in the mouse bed nucleus of the stria terminalis. Neuropharmacology 131, 83–95 (2017).
17. Ciccocioppo, R. et al. The bed nucleus is a neuroanatomical substrate for the anorectic effect of corticotropin-releasing factor and for its reversal by nociceptin/orphanin FQ. J. Neurosci. 23, 9445–9451 (2003).
18. Kocho-Schellenberg, M. et al. PACAP in the BNST produces anorexia and weight loss in male and female rats. Neuropsychopharmacology 39, 1614–1623 (2014).
原文链接:https://www.nature.com/articles/s41
如有相关需求,或了解更多产品服务,欢迎咨询我们!