武汉枢密脑科学技术有限公司品牌商
8 年
手机商铺
- NaN
- 0
- 0
- 1
- 0
武汉枢密脑科学技术有限公司
入驻年限:8 年
- 联系人:
枢先生
- 所在地区:
湖北 武汉市 江夏区
- 业务范围:
抗体、试剂、细胞库 / 细胞培养、技术服务、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 经销商
推荐产品
公司新闻/正文
2021 年度好文盘点!-神经科学
3938 人阅读发布时间:2023-06-13 15:47
2021 年,枢密客户共发表文章 110 余篇,总影响因子高达 1087.934,多篇优秀成果发表在《Nature》、《Cell》、《Nature Neuroscience》、《Molecular Psychiatry》、《Nature Communications》、《Neuron》、《PNAS》等国际知名期刊。在此对大家取得的优秀成绩致以衷心的祝贺。同时,我们也衷心祝愿枢密客户,在虎年里再创佳绩,枢密将竭诚为您提供更高效、优质的产品,助力您勇攀科学高峰。
枢密科技自成立 8 年来,始终坚持以「严谨科学的精神,铸造优良的产品」为初心,专注于病毒载体技术及转化医学研究服务。为国内外 20 +家药企、400 +卓越课题组、1600 +位科研工作者提供优质、高效、前沿的工具病毒和技术支持服务。在神经科学、神经系统疾病、基因功能研究、遗传疾病、基因治疗、肿瘤、干细胞治疗等转化医学领域提供高品质病毒载体产品和实验研究服务,获得了一线研究人员的高度认可。
2021 年枢密科技客户代表性文章
《Nature Neuroscience》,IF:24.884
Distinct thalamocortical circuits underlie allodynia induced by tissue injury and by depression-like states

通讯作者(单位):张智教授、晋艳教授、李娟教授 中国科学技术大学、中科大一附院
枢密产品:rAAV-Ef1α-DIO-EGFP-WPRE-pA,rAAV-Ef1α-DIO-RVG-WPRE-pA,RV-EnvA-ΔG–DsRed,rAAV-Ef1α-DIO-hChR2(H134R)-mCherry-WPRE-pA,rAAV-Ef1α-DIO-eNpHR3.0 -EYFP-WPRE-pA,rAAV-Ef1α-DIO-hM4D(Gi)-mCherry-WPRE-pA,rAAV-Ef1α-DIO-hM3D(Gq)-mCherry-WPRE-pA,rAAV-CaMK2a-hM3D(Gq)-mCherry-WPRE-pA,rAAV-Ef1α-DIO-mCherry-WPRE-pA,rAAV-DIO-EYFP-WPRE-pA,rAAV-CaMK2a-mCherry-WPRE-hGH-pA,rAAV-CaMK2a-EYFP-WPRE-pA,rAAV-DLX5 / 6 -mCherry-WPRE-hGH,retro-AAV-CaMK2a-Cre-WPRE-pA,retro-AAV-hSyn-Cre-WPRE-pA,rAAV-Ef1α-DIO-GCaMP6m-WPRE-pA,retro-AAV-CaMK2a-EGFP-WPRE-hGH,retro-AAV-hSyn–EGFP-WPRE-hGH
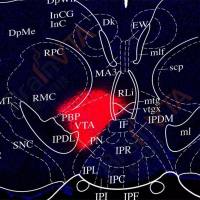
导读:人类的组织损伤和抑郁都能导致痛觉超敏,但这是否涉及不同的神经回路尚不清楚。本文作者在雄性小鼠中鉴定了两个离散的谷氨酸能神经元回路:丘脑后核(POGlu)到初级体感皮层谷氨酸能神经元(S1Glu)的投射介导组织损伤引起的痛觉超敏,而从束旁丘脑核(PFGlu)到前扣带皮层 GABA 能神经元再到谷氨酸能神经元(ACCGABA→Glu)的通路介导了与抑郁样状态相关的痛觉超敏。体内钙成像和多极电生理记录显示,POGlu和 PFGlu的神经元群在这两种情况下经历了不同的适应。人工操作每一个回路都会影响由组织损伤或抑郁样状态引起的痛觉超敏,但不能同时影响两者。作者研究表明不同的丘脑皮层回路 POGlu→S1Glu和 PFGlu→ACCGABA→Glu分别与组织损伤和抑郁样状态的阈下痛觉超敏相关,从而提供了对不同病因引起的病理性疼痛回路的基础见解。
《Nature Communications》,IF:14.919
A brainstem reticulotegmental neural ensemble drives acoustic startle reflexes

通讯作者(单位):熊伟教授 中国科学技术大学生命科学与医学部
枢密产品:rAAV-hSyn-hChR2(H134R)-EGFP-WPRE-pA,rAAV-hSyn-EGFP-WPRE-pA,rAAV-hSyn-Cre-EGFP-WPRE-pA,rAAV-EFlα-flex-taCasp3 -TEVp-WPRE-pA,rAAV-EF1α-DIO-EGFP-WPRE-pA,rAAV-EFlα-DIO-Gcamp6m-WPRE-pA,rAAV-EF1α-DIO-mCherry-WPRE-pA,rAAV-EF1α-DIO-hChR2(H134R)-EGFP-WPRE-pA,rAAV-EF1α-DIO-mGFP- 2A-Synaptophysin-mCherry-WPRE-pA,Retro-AAV-hSyn-G-EGFP-WPRE-pA,RV-N2C-ΔG-mCherry
导读:网状被盖核(RtTg)长期以来被认为是脑干网状结构(RF)的重要组成部分。然而 RtTg 及其相关环路的功能仍不清楚。本文作者揭示了 RtTg 在惊跳反射(一种高度保守的先天性防御行为)中的作用。光遗传激活 RtTg 神经元引起小鼠强烈的惊跳反应。RtTg 中的谷氨酸能神经元在听觉惊跳反射(ASR)过程中被显著激活。化学遗传抑制 RtTg 中谷氨酸能神经元降低 ASR 振幅。病毒追踪揭示了 ASR 神经回路:耳蜗核携带听觉信息向 RtTg 中谷氨酸能神经元发送直接的兴奋性神经支配,而后者又投射到脊髓运动神经元。综上所述,这些发现描述了 RtTg 及其相关神经回路在惊跳反射中的功能作用,并证明了 RF 如何将听觉系统与运动功能联系起来。
《Neuron》,IF:17.173
Early-life inflammation promotes depressive symptoms in adolescence via microglial engulfment of dendritic spines

通讯作者(单位):张智教授、晋艳教授、徐林教授 中国科学技术大学、中国科学院大学
枢密产品:rAAV-EF1α-DIO-hM4D(Gi)-mCherry-WPRE-pA,rAAV-EF1α-DIO-hM3D(Gq)-mCherry-WPRE-pA,rAAV-EF1α-DIO-mCherry-WPRE-pA,rAAV-CaMKIIa-Cre-WPRE-hGH-pA,rAAV-CAG-DIO-mCherry-mCherry-WPREs,rAAV-EF1α-DIO-GCaMP6m-WPRE-hGH-pA,rAAV-CaMKIIa-GCaMP6f-WPRE-hGH pA,rAAV-CMV-DIO-EGFP-WPRE-hGH pA,rAAV-CMV-DIO-CX3CR1 - 2a-EGFP-WPRE-hGH pA,rAAV-U6 -Loxp-CMV-EGFP-Loxp-CX3CR1 shRNA-SV40 pA,rAAV-U6 -Loxp-CMV-EGFP-Loxp-scramble shRNA-SV40 pA
导读:生命早期的炎症增加了个体在青春期或成年后患上抑郁症的风险。本文作者研究揭示了早期炎症如何导致青春期抑郁样症状:通过改变小胶质细胞的长期神经元树突棘吞噬能力。出生后 14 天(P14)小鼠暴露于脂多糖(LPS),并通过 Toll 样受体 4 /NF-κB 信号通路诱导炎症,活体大脑纵向成像显示,生命早期(P14)炎症增加出生后 45 天的青春期过程中前扣带回皮层(ACC)谷氨酸能(ACCGlu)神经元树突棘周围小胶质细胞吞噬的程度。当 LPS 处理小鼠的 ACC 小胶质细胞被去除或受到化学抑制时,这些小鼠在青春期没有表现出抑郁样行为。此外,作者还发现趋化因子受体 CX3CR1 介导应激诱导的 ACCGlu神经元树突棘的吞噬。综上所述,这些研究结果证实,早期炎症导致小胶质细胞吞噬能力失调(编码 ACCGlu神经元对应激/压力的长期不适应),从而促进青春期抑郁样症状的发展。
《eLife》,IF:8.140
Dorsal raphe nucleus to anterior cingulate cortex 5 -HTergic neural circuit modulates consolation and sociability

通讯作者(单位):邰发道教授 陕西师范大学
枢密产品:rAAV(Retro)-TPH2 -Cre,rAAV-EF1α-DIO-ChR2 -mCherry,rAAV-EF1α-DIO-eNpHR3.0 -mCherry,rAAV-EF1α-DIO-mCherry,rAAV-EF1α-DIO-hM4D(Gi)-mCherry,rAAV-EF1α-DIO-hM3D(Gq)-mCherry,rAAV-hSyn- 5 HT2.1,rAAV-hSyn-EGFP,rAAV-EF1α-DIO-GCaMP6,rAAV-hSyn-DIO-EGFP
导读:安慰是人类和一些社会动物对他人痛苦的共同反应,但这种行为背后的神经机制还不是很清楚。通过使用一夫一妻制的棕色田鼠,本文作者研究发现光遗传或化学遗传抑制中缝背核(DR)中 5 -羟色胺(5 -HT)能神经元,或光遗传抑制前扣带回(ACC)5 -HT 末端显著减少安慰实验中相互理毛时间,显著降低三室实验中社交接触。在相互理毛、嗅探和社交接触过程中,ACC 内 5 -HT 的释放和 DR 神经元的活性显著增加。最后,作者发现 ACC 中 5 -HT1A 受体的激活足以逆转 DR 中 5 -羟色胺能神经元的化学遗传抑制引起的安慰和社交能力缺陷。总的来说,本文研究提供了 DR-ACC 5 -HT 能神经回路的第一个与安慰样行为和社交能力有关的直接证据。
《The Journal of Clinical Investigation》,IF:14.808
Extracellular matrix protein laminin β1 regulates pain sensitivity and anxiodepression-like behaviors in mice

通讯作者(单位):罗层教授、武胜昔教授 空军军医大学
枢密产品:rAAV2 / 9 -U6 -shRNA(scramble)-CMV-EGFP-SV40pA,rAAV2 / 9 -U6 -shRNA(Lamb1)-CMV-EGFP-SV40pA,LV-U6 -shRNA(Lamb1)-CMV-EGFP-WPRE,LV-U6 -shRNA(Scramble)-CMV-EGFP-WPRE,rAAV2 / 9 -U6 -shRNA(scramble)-CMV-mCherry-SV40pA,rAAV2 / 9 -U6 -shRNA(Lamb1)-CMV-mCherry-SV40pA,rAAV2 / 9 -CaMKIIa-GCaMP6s-WPRE-pA,rAAV2 / 9 -U6 -shRNA(ITGB1)-CMV-mCherry-SV40pA
导读:神经病理性疼痛患者通常会经历精神障碍的共病。前扣带回皮层(ACC)的细胞可塑性被认为是疼痛感知和情绪的关键界面。然而,到目前为止,大量的研究集中在细胞内的可塑性机制上,而不是可能触发和促进细胞内变化的细胞外改变。层粘连蛋白(Laminin)是细胞外基质(ECM)的关键组分,由一条α链、一条β链和一条γ链组成,参与多种病理生理过程。本文作者在小鼠中发现,ACC 中的层粘连蛋白β1(Laminin β1,LAMB1)在周围神经病变时显著下调表达。ACC 中 LAMB1 基因的敲除加重了疼痛敏感性并诱发焦虑和抑郁。机制分析表明,LAMB1 的缺失通过与整合素β1 的相互作用以及随后的 Src 依赖的 RhoA/LIMK/cofilin 途径引起肌动蛋白失调,导致突触前递质释放概率增加和异常突触后脊柱重塑,这反过来协调了锥体神经元的结构和功能可塑性,最终导致疼痛超敏反应和焦虑抑制。本研究揭示了 ECM LAMB1 在调节疼痛可塑性方面的功能能力,并确定了一种将细胞外的改变传递给细胞内的可塑性的机制。此外作者确定了扣带回 LAMB1 /整合素β1 信号是治疗神经性疼痛和相关焦虑抑制的一个有希望的治疗靶点。
《Signal Transduction and Targeted Therapy》,IF:18.187
STN–ANT plasticity is crucial for the motor control in Parkinson’s disease model

通讯作者(单位):王以政研究员 北京基础医学研究所
枢密产品:rAAV2 / 9 -CaMKⅡa-EYFP,rAAV2 / 1 -CaMKⅡa-Cre,rAAV2 / 9 -EF1α-DIO-EYFP,rAAV2 / 9 -CaMKⅡa-ChR2(H134R)-mCherry,rAAV2 / 9 -hSyn-eNpHR-YFP,rAAV2 / 9 -hSyn-eNpHR-YFP,rAAV2 / 9 -EF1α-DIO-eNpHR-EYFP
导读:帕金森病(PD)是一种由中脑黑质(SN)多巴胺能神经元退行性死亡导致纹状体中多巴胺水平降低,进而引起基底节活性异常的运动障碍性疾病。临床上常予以脑深部电刺激术(DBS)治疗改善基底节活性,DBS 靶点为丘脑底核(STN)及其下游核团苍白球内侧部(GPi)。二者治疗效果及副作用方面的诸多差异提示除 STN-GPi 外,存在其他环路参与运动控制和 PD 运动障碍的发生。作者通过顺行、顺行跨单级突触及逆行病毒示踪系统反复验证 ANT(丘脑前核)是 STN 尚未被报导的下游核团。进一步利用光遗传学偶联膜片钳技术发现 STN 与 ANT 之间存在功能上的兴奋性单突触连接。为探究 STN-ANT 环路在 PD 模型小鼠运动控制中的作用,作者利用光遗传学技术抑制 ANT 或 STN-ANT 环路,结果显示:给予黄光照射后能够改善 PD 小鼠运动障碍。最后,作者研究证明 STN-ANT 环路可塑性参与 PD 运动障碍发生。总之,作者首次发现了 STN-ANT 通路并证实了其可塑性参与调控 PD 模型鼠运动障碍的机制。
《PNAS》,IF:11.205
VLM catecholaminergic neurons control tumor growth by regulating CD8+T cells

通讯作者(单位):王晓东研究员 北京生命科学研究所
枢密产品:rAAV-EF1α-flex-taCasp3 -TEVp,rAAV-EF1α-DIO-mCherry,rAAV-hSyn-DIO-hM3D(Gq)-mCherry,rAAV-hSyn-DIO-hM4D(Gi)-mCherry
导读:众所周知,肿瘤的生长会受到神经系统的影响。然而,目前尚不清楚肿瘤是否能直接与中枢神经系统(CNS)沟通,或者是否这种相互作用可能影响肿瘤生长。本文作者研究表明荷瘤小鼠大脑中延髓腹外侧区(VLM)儿茶酚胺能(CA)神经元被激活,这些神经元的活性显著改变多种同系和自发小鼠肿瘤模型中的肿瘤生长。通过多巴胺-β-羟化酶(DBH)启动子激活 Dbh-Cre 小鼠的促凋亡因子 caspase- 3,从而特异性消融 VLM CA 神经元,以及通过化学遗传学方法抑制这些神经元,均可减缓肿瘤进展。相反地,化学遗传激活 VLM CA 神经元促进了肿瘤生长。VLM CA 神经元消融的肿瘤抑制作用在 Dbh-Cre;Rag1−/−小鼠中被削弱,表明这种调控作用是由适应性免疫系统介导的。进一步发现用抗 CD8+抗体特异性耗尽 CD8+T 细胞也减轻了 VLM CA 神经元消融对肿瘤的抑制作用。另外,还发现 VLM CA 神经元消融和紫杉醇治疗具有叠加的抗肿瘤效果。总之,以上结果提示了一条 VLM CA→CD8+T 细胞→肿瘤的调控通路,可能参与到抑制肿瘤的过度生长过程,揭示了小鼠大脑中 VLM CA 神经元在控制小鼠体内肿瘤生长中的作用。
《Alzheimers & Dementia》,IF:21.566
Nonenzymatic function of DPP4 in diabetes-associated mitochondrial dysfunction and cognitive impairment

通讯作者(单位):郑天鹏教授 桂林医学院第二附属医院
枢密产品:AAV-shRNA-PAR2、AAV-shRNA-GLP- 1R、AAV-shRNA-control
导读:二肽基肽酶- 4(DPP4)已被证明通过酶和非酶途径发挥其功能。DPP4 在糖尿病相关认知障碍中的非酶功能尚不清楚。本研究中作者测定了 2 型糖尿病患者和 db/db 小鼠 DPP4 蛋白浓度或酶活性,并在体内和体外测试 DPP4 的非酶功能对线粒体功能障碍和认知功能障碍的影响。结果表明,DPP4 活性升高是 2 型糖尿病患者偶发轻度认知损害(MCI)的独立危险因素。此外,DPP4 在 db/db 小鼠海马中高度表达,并导致线粒体功能障碍和认知功能障碍。在机制上,DPP4 可能与海马中的 PAR2 结合并触发 GSK- 3β激活,下调过氧化物酶体增殖物激活受体γ-辅激活因子 1α(PGC- 1α)表达,导致线粒体功能障碍,从而促进糖尿病患者的认知障碍。总体而言,这些研究结果表明,DPP4 的非酶功能可能促进糖尿病患者的线粒体功能障碍和认知功能障碍。
《Nature》,IF:49.962
The mouse cortico-basal ganglia-thalamic network

通讯作者(单位):Foster Nicholas N. 教授、Dong Hong-Wei 教授 南加州大学凯克医学中心
枢密产品:rAAV-EFlα-DIO-GFP、rAAV-CMV-Cre
导读:皮质-基底核-丘脑-皮质环路是大脑中的基本网络基序之一。揭示其结构和功能组织对于理解认知、感觉运动行为以及许多神经和神经精神疾病的自然史至关重要。经典地,这个网络被概念化为包含三个信息通道:运动、边缘和联想。然而,这三个通道的观点不能解释基底核的无数功能。作者之前根据整个皮质的输入图谱将背侧纹状体细分为 29 个功能区。而本研究中作者绘制了这些纹状体区域通过苍白球外侧部分(GPe)、黑质网状部分(SNr)、丘脑核和皮质的多突触输出通路。因此,确定了 14 个 SNr 和 36 个 GPe 区域以及一条直接的皮质-SNr 投射。尽管来自同一纹状体区域的直接和间接通路最终汇聚到相同的突触后 SNr 神经元上,但纹状体-神经节直接通路比平行的纹状体-神经节间接通路显示出更大的纹状体输入汇合。根据 SNr 输出,研究人员在丘脑束旁核和腹内侧核描绘了 6 个区域。随后,确定了 6 个平行的皮质-基底神经节-丘脑子网络,它们通过皮质-基底神经节-丘脑环路的每个基本节点依次传递特定的皮质信息子集。丘脑区域以真正的闭环形式将这一输出传递回每个子网络的原始皮质层神经元。
《Cell》,IF:41.582
Iterative tomography with digital adaptive optics permits hour-long intravital observation of 3D subcellular dynamics at millisecond scale

通讯作者(单位):戴琼海院士、范静涛研究员、俞立教授 清华大学自动化系脑与认知科学研究所、生命科学学院
枢密产品:rLV-EF1α-GCamp6s-WPRE
导读:哺乳动物的长期亚细胞活体内成像对于研究自然生理过程中不同的细胞间行为和细胞器功能至关重要。然而光学异质性、组织不透明性和光毒性带来了巨大的挑战。本研究中作者提出了一种计算成像框架,称为数字自适应光学扫描光场相互迭代层析成像(DAOSLIMIT),具有高速、高分辨率 3D 成像、平铺波前校正和紧凑系统的低光毒性特性。通过同时对整个体积进行断层成像,研究人员获得了 225×225×16μm3的体积成像,横向分辨率高达 220nm,轴向分辨率高达 400nm,毫秒级,超过数十万个时间点。为建立这种能力,作者研究了不同物种的大规模细胞迁移和神经活动,并观察了哺乳动物中性粒细胞迁移和肿瘤细胞循环过程中的各种亚细胞动力学。
《Nature methods》,IF:28.547
High-definition imaging using line-illumination modulation microscopy

通讯作者(单位):骆清铭院士、袁菁教授 海南大学生物医学工程学院、武汉光电国家研究中心
枢密产品:RV-ΔG-GFP
导读:通过光学显微镜对大规模三维(3D)样品进行显微可视化需要克服成像质量和速度以及大数据采集和管理方面的挑战。本研究中作者报告了一种线照明调制(LiMo)技术,用于高吞吐量和低背景厚组织成像。将 LiMo 与薄组织切片相结合,研究人员进一步开发了一种高清晰度荧光显微光学切片层析成像(HD-fMOST)方法,其平均信噪比为 110,促进了神经元形态重建的实质性改善。以 0.32 × 0.32 × 1.00 μm3的体素分辨率实现了>30 倍的无损数据压缩 ,完成了在线数据存储到 U 盘或云盘,以及高精度(95% 准确度)全脑 3D 细胞实时计数。总的来说,这些结果突出了 HD-fMOST 促进全脑高分辨率数据集的大规模采集和分析的潜力。
《Nature Neuroscience》,IF:24.884
A neural circuit for excessive feeding driven by environmental context in mice

通讯作者(单位):Fu Yu 教授、Mohammad Hasan 教授 新加坡国立大学、新加坡科学技术研究局(A*STAR)
枢密产品:AAV9 -EF1α-DIO-GCaMP6m
导读:尽管有明显的遗传影响,肥胖主要还是由过度摄入食物引起的,而过度摄入食物是由生理、认知和环境因素的相互作用引起的。在肥胖患者中,饮食更多地取决于外部线索,而不是内在生理需求。然而,环境背景如何驱动非稳态进食尚不清楚。本研究中作者鉴定出小鼠下丘脑结节核内的生长抑素(TNSST)神经元群,这些神经元优先被可口的食物激活。TNSST 神经元的激活使得在饱食小鼠中驱动非稳态进食成为可能,并且需要来自海马下托的输入。予以小鼠可口的食物的环境,极大地增强了海马下托和 TNSST 神经元之间的突触传递,并驱动了非稳态进食。这种进食可以通过抑制 TNSST 神经元或海马下托但不抑制其他主要的促食欲神经元而被选择性抑制。综上所述,这些结果通过特定的下丘脑环路揭示了适口食物的环境背景如何驱动非稳态进食。
《Cell Reports》,IF:9.423
Oxytocin in the anterior cingulate cortex attenuates neuropathic pain and emotional anxiety by inhibiting presynaptic long-term potentiation

通讯作者(单位):卓敏院士 加拿大皇家科学院
枢密产品:AAV-DIO-ChR2 -EYFP,AAV-DIO-EYFP,AAV-DIO-eNpHR3.0 -mCherry
导读:催产素是一种众所周知的神经垂体激素,在焦虑行为和伤害感受中起着重要作用。前扣带皮层(ACC)中存在两种主要形式的长时程增强,即突触前 LTP(前-LTP)和突触后 LTP(后-LTP)。前-LTP 和后-LTP 都会导致慢性疼痛相关焦虑和行为敏化。催产素在 ACC 中的作用尚未被研究。本文作者发现在患有神经病理性疼痛的动物中,向 ACC 内微量注射催产素可以减弱伤害性反应和焦虑样行为反应。应用催产素可选择性阻断前-LTP 的维持,但不会阻断后-LTP 的维持。此外,催产素可增强抑制性传递并兴奋 ACC 中间神经元。在患有神经病理性疼痛的动物中,通过选择性光学刺激 ACC 内含有催产素的投射末端,也获得了类似的结果。总的来说,这些结果证明催产素作用于中枢突触,并通过减少前-LTP 而减轻慢性疼痛引起的焦虑。
《Current Biology》,IF:10.834
The NAergic locus coeruleus-ventrolateral preoptic area neural circuit mediates rapid arousal from sleep

通讯作者(单位):张玲教授、王烈成教授 同济大学医学院、安徽医科大学
枢密产品:rAAV-mTH-NLS-Cre,rAAV-EF1α-DIO-hChR2(H134R)-eYFP,rAAV-EF1α-DIO-eNpHR3.0 -eYFP
导读:蓝斑核(LC)位于脑干,在促进觉醒方面起着重要作用。然而,这一功能背后的神经回路仍不清楚。使用皮质脑电图结合光电管记录,本文作者发现 LCNA 神经元在清醒时表现出高活性,而抑制这些神经元的活动会导致清醒度降低。病毒追踪显示 LCNA 神经元直接投射到下丘脑腹外侧视前区(VLPO),光遗传激活 NAergic LC-VLPO 神经回路促进觉醒。VLPO 中的光电二极管记录显示响应于光遗传激活 LCNA 神经元,两个功能不同的神经元群被刺激。随后,作者鉴定了两种类型的 VLPO 神经元,它们对不同受体介导的 LC NAergic 投射表现出不同的反应 。总之,这些研究结果表明,NAergic LC-VLPO 神经回路是一个重要的控制清醒的神经通路,通过α2 受体抑制 VLPO 中的睡眠活跃神经元,以及通过α1 受体和β受体激活 VLPO 中的觉醒活跃神经元,从而产生协同效应。
《Cell Reports》,IF:9.423
Deficiency of ER Ca2 + sensor STIM1 in AgRP neurons confers protection against dietary obesity

通讯作者(单位):张果教授、吕义晟教授 华中科技大学同济医学院
枢密产品:rAAV-Eflα-DIO-GCaMP6m-WPRE-hGH-polyA
导读:SOCE(钙池调控钙离子进入)是维持细胞内 Ca2 +水平和细胞功能的关键,然而,它在肥胖症发展中的作用仍不清楚。本文作者研究发现基质相互作用分子 1[Stim1,SOCE 的内质网(ER)Ca2 +传感器] 与肥胖的发展密切相关。大脑中 SOCE 的药理学阻断,或下丘脑刺鼠相关肽(AgRP)产生神经元中 Stim1 的破坏(ASKO),显著改善饮食肥胖及其相关的代谢紊乱。相反地,AgRP 神经元中 Stim1 的组成性激活导致肥胖样表型。作者还发现阻断 SOCE 可通过 Oas3(2',5'-寡腺苷酸合成酶 3)-RNase(核糖核酸酶)L 信号通路抑制神经细胞中的一般性翻译。而 AgRP 神经元中 Oas3 的过度表达可保护小鼠免受饮食肥胖,这些神经元中 RNase L 的失活显著消除了 ASKO 的作用。总的来说,这些发现强调了 Stim1 和 SOCE 在肥胖发展中的重要作用。
《BRAIN》,IF:13.501
GPR151 in nociceptors modulates neuropathic pain via regulating P2X3 function and microglial activation

通讯作者(单位):徐贞仲教授 浙江大学
枢密产品:AAV9 -sgRNA
导读:神经病理性疼痛是一个影响着全世界 7 - 10% 的人口的主要的健康问题。目前,神经病理性疼痛由于其难以捉摸的机制而难以治疗。本文作者发现伤害性感觉神经元中的孤儿 G 蛋白偶联受体 151(GPR151)控制由神经损伤引起的神经病理性疼痛。GPR151 主要表达于非肽能 C 纤维背根神经节(DRG)神经元,并在神经损伤后高度上调表达。重要的是,成熟伤害性感觉神经元中 Gpr151 的条件性敲除显著减轻慢性压迫性神经损伤(CCI)诱导的神经病理性疼痛样行为,但不影响基础伤害性感觉。此外,DRG 神经元中的 GPR151 是 CCI 诱导的神经元过度兴奋及集落刺激因子 1(CSF1)的上调表达所必需的,而这些都是神经损伤后脊髓小胶质细胞激活所必需的。在机制上,GPR151 与 P2X3 离子通道偶联,并促进其在神经病理性疼痛样超敏反应中的功能活动。敲除 Gpr151 可抑制 P2X3 介导的钙离子浓度升高和 CCI 小鼠的自发疼痛行为。相反,Gpr151 的过度表达显著增强了 P2X3 介导的钙离子浓度升高和 DRG 神经元兴奋性。此外,DRG 中 P2X3 的敲除逆转了 CCI 诱导的 CSF1 上调表达、脊髓小胶质细胞激活和神经病理性疼痛样行为。最后,GPR151 和 P2X3 在小直径人 DRG 神经元中的共表达得到证实,表明这些发现的临床相关性。总之,这些研究结果表明,伤害性 DRG 神经元中的 GPR151 在神经病理性疼痛的发病机制中起着关键作用,并可能成为治疗神经病理性疼痛的潜在靶点。